时间:2020-08-23 06:03:19
1、选择题 用水稀释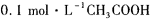 时,溶液中随着水量的增加而减小的是
时,溶液中随着水量的增加而减小的是
A.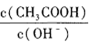
B.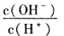
C.c(H+)和c( OH-)的乘积
D.OH-的物质的量
2、选择题 下列各溶液中,微粒的物质的量浓度关系正确的是
A.0.1 mol·L-1 Na2CO3溶液:c(Na+)=2c(HCO3-)+2c(CO32-)+2c(H2CO3)
B.0.1 mol·L-1 NH4Cl溶液:c(NH4+)=c(Cl-)
C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+) > c(CH3COO-) > c(H+) > c(OH-)
D.常温下,将pH=2的盐酸和pH=12的氨水等体积混合后:c(NH4+) > c(Cl-) > c(OH-) > c(H+)
3、选择题 常温时,下列叙述正确的是
A.pH=9的NH4Cl与NH3·H2O混合溶液中c(Cl-)>c(NH4+)
B.pH=2.5的可乐中c(H+)是pH=3.5的柠檬水中c(H+)的1 0倍
C.AgCl在0.1 mol/L CaCl2溶液和0.l mol/L NaCl溶液中的溶解度相同
D.1 mL l mol l L Na2CO3溶液加水稀释至100 mL,pH和Kw均减小
4、选择题 下列图示与对应的叙述相符的是: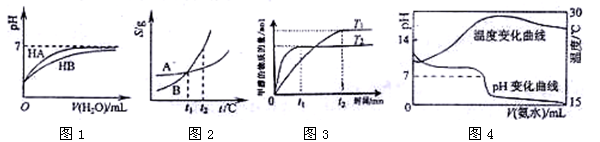
A.图1表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH小于同浓度的NaB溶液的pH。
B.图2表示A、B两物质的溶解度随温度变化情况,将t1℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数 B
5、选择题 常温下,向l00mL 0.01mol/L HA的溶液中逐滴加入0.02mol/L MOH溶液,如图所示,曲线表示混合溶液的pH变化情况(溶液体积变化忽略不计)。下列说法中不正确的是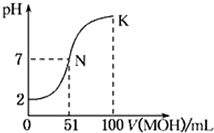
A.HA为一元强酸
B.N点水的电离程度小于K点水的电离程度
C.随着MOH溶液的滴加,比值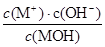 不变
不变
D.若K点对应的溶液的pH=10,则有c(MOH)+c(OH-)-c(H+)=0.005mol/L