时间:2020-08-13 07:22:27
1、选择题 已知 1mol白磷转化为红磷时放出 18.39 kJ的热量。在下列两个反应中:
4P(白、s)+ 5O2(g)=2P2O5(s);ΔH = -a kJ/mol(a > 0)
4P(红、s)+ 5O2(g)=2P2O5(s);ΔH = -b kJ/mol(b> 0)
a和b的关系为
[? ]
A.a < b
B.a = b
C.a > b
D.无法确定
2、选择题 根据下列热化学方程式
(1)C(s)+O2(g)=CO2(g)△H1=-393.5kJ/mol
(2)H2(g)+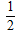 O2(g)=2H2O(l)△H2=-285.8kJ/mol
O2(g)=2H2O(l)△H2=-285.8kJ/mol
(3)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l)△H3=-870.3kJ/mol
可以计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热为( )
A.△H=244.1kJ/mol
B.△H=-488.3kJ/mol
C.△H=-996.6kJ/mol
D.△H=996.6kJ/mol
3、填空题 NO2被誉为生命的“信息分子”,铵盐为植物生长的“食物”,氮及其化合物在工农业生产和生命活动中起着重要的作用。
(1)在100℃时,将0.100 mol的N2O4气体充入1L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到下表数据: 
①从表中分析:该温度下,反应N2O4(g) 2NO2(g) 的平衡常数为_______,N2O4的转化率为______。
2NO2(g) 的平衡常数为_______,N2O4的转化率为______。
②在上述条件下,60s内N2O4的平均反应速率为__________mol/(L·s)。
③达平衡后下列条件的改变可使NO2浓度增大的是__________
A.增大容器的容积
B.再充入一定量的N2O4
C.再充入一定量的NO2
D.再充入一定量的He
(2)氨气与硝酸反应可生成硝酸铵,NH4NO3热分解反应的方程式及反应热分别为(注:kJ/g也是反应热的单位):
NH4NO3(s)=N2O(g)+2H2O (l) △H=-0.53 kJ/g ①
NH4NO3(s)=N2(g)+1/2O2(g)+2H2O(l) △H=-1.47 kJ/g ②
则2N2O(g)=2N2(g)+O2(g)的△H=__________kJ/mol。
4、选择题 已知:
(1)Zn(s)+1/2O2(g)=ZnO(s) ΔH=-348.3kJ/mol
(2)2Ag(s)+1/2O2(g)=Ag2O(s) ΔH=-31.0kJ/mol
则ZnO(s)+2Ag(s)=Zn(s)+Ag2O(s)的ΔH等于
[? ]
A.-317.3kJ/mol
B.+379.3kJ/mol
C.-332.8kJ/mol
D.+317.3 kJ/mol
5、选择题 S(单斜)和S(正交)是硫的两种同素异形体。
已知:
① S(单斜,s)+O2(g) == SO2(g) △H1=-297.16 kJ·mol-1
② S(正交,s)+O2(g) == SO2(g) △H2=-296.83 kJ·mol-1
③ S(单斜,s) == S(正交,s) △H3 下列说法正确的是
[? ]
A.△H3=+ 0.33 kJ·mol-1
B.单斜硫转化为正交硫的反应是吸热反应
C.S(单斜,s) == S(正交,s) △H3<0,正交硫比单斜硫稳定
D.S(单斜,s) == S(正交,s) △H3>0,单斜硫比正交硫稳定