时间:2020-08-13 07:15:38
1、填空题 已知H2(g)、CO(g)和CH3OH(l)的燃烧热分别为285.8 kJ・mol-1、283.0 kJ・mol-1和726.5 kJ・mol-1。请回答下列问题。
(1)用太阳能分解5 mol液态水消耗的能量是 kJ。
(2)液态甲醇不完全燃烧生成一氧化碳气体和液态水的热化学方程式为 。
(3)在以甲醇为燃料的燃料电池中,电解质溶液为酸性,则正极的电极反应式为 。
理想状态下,该燃料电池消耗2 mol甲醇所能产生的最大电能为1 404.2 kJ,则该燃料电池的理论效率为 。(燃料电池的理论效率是指电池所产生的最大电能与燃料电池反应所能释放的全部能量之比)
参考答案:(1)1 429
(2)CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH=-443.5 kJ・mol-1
(3)O2+4e-+4H+=2H2O 96.6%
本题解析:(1)根据能量守恒定律可知分解5 mol液态水消耗的能量与生成5 mol液态水放出的能量相等,285.8 kJ・mol-1×5 mol=1 429 kJ。
(2)2CO(g)+O2(g)=2CO2(g) ΔH=-566.0 kJ・mol-1 ①
2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 453.0 kJ・mol-1 ②
根据盖斯定律(②-①)÷2得:CH3OH(l)+O2(g)=CO(g)+2H2O(l) ΔH=-443.5 kJ・mol-1。
(3)甲醇燃料电池的正极反应物为O2,酸性条件下生成H2O:O2+4e-+4H+=2H2O。2 mol甲醇完全燃烧放出的热量为1 453.0 kJ,故该电池的理论效率为1 404.2 kJ÷1 453.0 kJ×100%=96.6%。
本题难度:一般
2、选择题 如图所示的装置能形成原电池的是
参考答案:D
本题解析:略
本题难度:简单
3、选择题 如图有关电化学的图示,完全正确的是( )
A.
Cu-Zn原电池
B.
粗铜的精炼
C.
铁片镀锌
D.
验证NaCl溶液(含酚酞)电解产物
参考答案:A、原电池中较活泼的金属作负极,较不活泼的金属或导电的非金属作正极,所以铜-锌-稀硫酸原电池中,锌作负极铜作正极,故A错误;
B、粗铜的精炼中,粗铜作阳极,纯铜作阴极,电解质溶液为含有铜离子的盐,故B错误;
C、电镀时,镀层作阳极,镀件作阴极,所以铁片上镀锌,锌作阳极,铁作阳极,故C错误;
D、电解时,电流流入的电极为阳极,另一电极为阴极,所以电解氯化钠溶液时,根据图片知,碳棒为阳极,铁棒为阴极,阳极上氯离子失电子生成氯气,氯气能置换碘化钾中的碘,碘遇淀粉变蓝色,所以阳极上用淀粉碘化钾溶液可检验氯气的存在;阴极上氢离子得电子生成氢气,利用氢气的燃烧实验检验阴极产物;溶液中有氢氧化钠产生,无色酚酞试液遇碱变红色,所以可用无色酚酞检验氢氧化钠的生成,故D正确;
故选D.
本题解析:
本题难度:一般
4、填空题 (12分)(1).下列有关电化学的图示中,完全正确的是?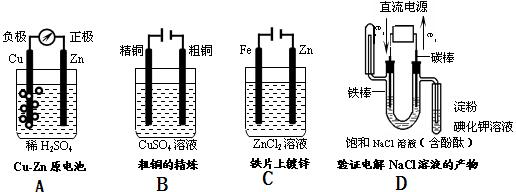
(2).碘被称为“智力元素”,科学合理地补充碘可防止碘缺乏病。碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中可与碘化物作用生成单质碘。以碘为原料,通过电解制备碘酸钾的实验装置如图所示。
请回答下列问题:
a、碘是?(填颜色)固体物质,实验室常用?方法来分离提纯含有少量泥沙杂质的固体碘。
b、电解前,先将一定量的精制碘溶于过量氢氧化钾溶
液,溶解时发生反应:3I2+6KOH==5KI+KIO3+3H2O,
将该溶液加入阳极区。另将氢氧化钾溶液加入阴极区,电解槽用水冷却。
电解时,阳极上发生反应的电极反应式为?,每生成1mol KIO3,电路中通过的电子的物质的量为___________________。
c、电解过程中,为确定电解是否完成,需检验电解液中是否有I-。请设计一个检验
电解液中是否有I-的简单实验方案,并按要求填写下表。
可供选择的试剂有淀粉溶液,稀硫酸,氯化钠溶液,酒精等。(用其中的一种或多种均可。)
| 实验方法 | 实验现象及结论 |
| ? | ? |
参考答案:(12分)
a、紫黑色(1分)升华(或加热)(1分)b、
(2分),6mol(1分) c、
实验方法
实验现象及结论
取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝。
如果不变蓝,说明无I-,;若变蓝,说明有I-。
d、冷却结晶,干燥,洗去吸附在碘酸钾晶体上的氢氧化钾等杂质。
本题解析:略
本题难度:一般
5、选择题 锂电池是新一代高能电池,目前已研究成功多种锂电池。某种锂电池的总反应式为:
Li + MnO2===LiMnO2。下列说法中正确的是?(?)
A.MnO2是负极,Li是正极
B.放电时负极的反应:Li - e― = Li+
C.放电时正极的反应:MnO2― - e― = MnO2
D.电池放电时,产生高锰酸根离子
参考答案:B
本题解析:略
本题难度:一般