ʱ��:2020-08-13 06:54:31
1��ѡ���� ����������ȼ�ϵ��Ϊ��Դ���е���ʵ��װ��ʾ��ͼ������ͼ��ʾ������˵���У���ȷ����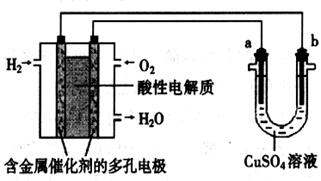
A����a����ͭ��b��Ϊ��ʱ�����������1.6g O2��b��������6.4gͭ
B��ȼ�ϵ�ع���ʱ��������ӦΪ��O2 + 2H2O + 4e-�� 4OH-
C����a���Ǵ�ͭ��b���Ǵ�ͭʱ��a�����ٵ���������b��������ͭ��������
D����a��b��������ʯīʱ��b����ӦΪ4OH- - 4e-��O2��+ 2H2O
�ο��𰸣�D
����������������֪����ͨ��������һ��Ϊ������bΪ������ͨ��������һ��Ϊ����������a��Ϊ������A��ȷ����a����ͭ��b��Ϊ������a����Cu�ܽ⣬��b�����������ݴ�����·����������ȣ�����֪��������1.6g O2����ת����0.2mol���ӣ�������0.1molͭ��������6.4gͭ��B����Ӧ��Ϊ
O2��2H�� + 2e-=2OH-��C������a���Ǵ�ͭ��b���Ǵ�ͭʱ��a�����ٵ�������һ����b��������ͭ��������ȣ���Ϊ��ͭ�������������ʣ�D����Ӧ����a������4OH- - 4e-��O2��+ 2H2O��
���������⿼����ԭ��ء����ص��ۺ�֪ʶ�������ⷽʽ�Ǹ߿�������ȵ㣬������һ�����ۺ��ԣ���һ�����Ѷȡ�
�����Ѷȣ���
2��ѡ���� ���и���װ���������ԭ��ص��ǣ�������
A��
ϡ����
B��
CuSO4��Һ
C��
�ƾ���Һ
D��
? ϡ����? ϡ����
�ο��𰸣�A�����缫�Ļ�������ͬ�����Բ��ܹ���ԭ��أ���A����
B������ԭ��صĹ��������������ܹ���ԭ��أ���B��ȷ��
C���ƾ��Ƿǵ���ʣ���װ�ò����Է��Ľ���������ԭ��Ӧ�����Բ��ܹ���ԭ��أ���C����
D����װ�ò����γɱպϻ�·�����Բ��ܹ���ԭ��أ���D����
��ѡB��
���������
�����Ѷȣ�һ��
3������� ij��Ӧ�з�Ӧ�����������У�FeCl2��FeCl3��CuCl2��Cu��
��1����������Ӧ��Ƴɵ�ԭ�����ͼ����ʾ����ش��������⣺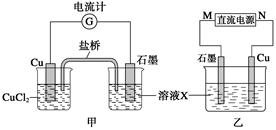 ?
?
��ͼ��X��Һ��?��
��ʯī�缫�Ϸ����ĵ缫��ӦʽΪ?��
��ԭ��ع���ʱ�������е�?(�K������Cl����)���Ͻ���X��Һ�С�
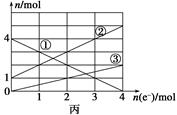
��2����������Ӧ��Ƴɵĵ�����ͼ����ʾ�����ձ��н��������ӵ����ʵ��������ת�Ƶ����ʵ����ı仯��ϵ��ͼ������ش��������⣺
��M��?����?��ͼ���еĢ�����?�ı仯��
�۵�����ת��Ϊ2 molʱ�������ձ��м���??L 5 mol��L��1 NaOH��Һ����ʹCu2+������ȫ��
��3��������Ҫ�������������(Na2FeO4)��һ����������ˮ�����������кܶ��ŵ㡣
�ٸ���������������֮һ�ǵ�ⷨ����ԭ��ΪFe��2NaOH��2H2O Na2FeO4��3H2��������ʱ�����ĵ缫��Ӧʽ��?��
Na2FeO4��3H2��������ʱ�����ĵ缫��Ӧʽ��?��
�ڸ���������������֮������ǿ���Խ�������NaClO����Fe(OH)3���ɸ������ơ��Ȼ��ƺ�ˮ���÷�Ӧ�����ӷ���ʽΪ?��
�ο��𰸣�(1) ��FeCl3��FeCl2?��Fe3++e-��Fe2+��K��? (2)�ٸ�
��Fe2��������FeCl2����2.8? (3)��Fe��8OH����6e����FeO42-��4H2O
��2Fe(OH)3��3ClO����4OH����2FeO42-��3Cl����5H2O
�����������1���ٸ÷�ӦӦ����Cu+2FeCl3=CuCl2+2FeCl2������ͭ�ǻ�ԭ�����������������Ȼ����õ����ӱ���ԭΪ�Ȼ�����������װ����XӦ����FeCl3��FeCl2��
��ʯī�������������ӵõ����ӣ��缫�Ϸ����ĵ缫��ӦʽΪFe3++e-��Fe2+��
��ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ����˸�ԭ��ع���ʱ�������е�K�����Ͻ���X��Һ�С�
��2���ٸ��ݱ�ͼ��֪��Һ�������ֽ��������ӣ�������X�ijɷֿ�֪X��ֻ�����ֽ��������ӣ�˵���ڵ������л���Cu2+���ɣ����Cu��������ʯī������������MΪ������NΪ������
�ڸ���ת�Ƶ��ӵ����ʵ����ͽ��������ӵ����ʵ����ı仯����֪��ΪFe3+����ΪFe2+����ΪCu2+���۵�����ת��Ϊ2molʱ����Һ����Fe3+ 2mol��Fe2+ 3mol��Cu2+Ϊ1mol��������Ҫ����NaOH��Һ14mol�����NaOH��Һ�����Ϊ14mol��5mol/L��2.8L��
��3���ٵ��ʱ��������������Ӧ���缫��Ӧ����ʽΪFe+8OH--6e-�TFeO42-+4H2O��
��NaClO����Fe��OH��3�ķ�Ӧ����ʽΪ2Fe��OH��3+3ClO-+4OH-�T2FeO42-+3Cl-+5H2O��
�����Ѷȣ���
4��ѡ���� ���и���ʵ��װ���ܴﵽʵ��Ŀ���ǣ�������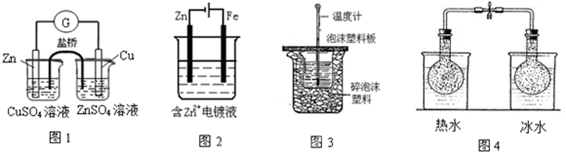
A����ͼ1��ʾװ�����пͭԭ���
B����ͼ2��ʾװ���������϶�п
C����ͼ3��ʾװ�òⶨϡ�����ϡNaOH��Ӧ���к���
D����ͼ4��ʾװ���о��¶ȶ�2NO2��g��?N2O4��g��ƽ���Ӱ��
�ο��𰸣�A���������ŵ�ԭ����У��缫���Ϻ͵������Һ�н������ӱ�������ͬԪ�أ���ͼ�н������Ϻ͵������Һ�н��������Ӳ�����ͬԪ�أ����Բ��ܹ���ԭ��أ���A����
B���������϶�пʱ��п����������������������B����
C��ȱ�ٲ���������������������Һ�ᵼ����Һ�¶Ȳ����ȣ������к��Ȳ�ȷ����C����
D�����������Ǻ���ɫ���壬��������������ɫ���壬��ͬһ��Ӧװ�õĿ��淴Ӧ�У������¶Ȳ�ͬ����������ɫ�IJ�ͬȷ���¶ȶԿ��淴Ӧ��Ӱ�죬��D��ȷ��
��ѡD��
���������
�����Ѷȣ���
5������� ��12�֣�����ͼװ�ý���ʵ�飬���ش���������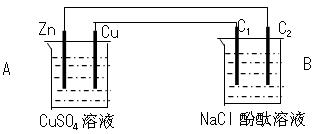
(1)�ж�װ�õ����ƣ�A��Ϊ___________ , B��Ϊ______________
(2)п��Ϊ__________�����缫��ӦʽΪ_______________?__________
(3)ʯī��C1Ϊ______�����缫��ӦʽΪ__________?_____________
ʯī��C2����������ʵ������Ϊ________________?____________
(4)��C2������224mL���壨��״̬��ʱ��п����������_________g��
�ο��𰸣�(12��)
��1��ԭ��أ�����
��2����? Zn - 2e- = Zn2+?��3����? 2 Cl- - 2e- = Cl2��
�缫�������ݲ�������ɫ��Һ���ɫ?��4��0.65
�����������
�����Ѷȣ���