时间:2020-08-13 06:46:36
1、填空题 某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液.盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如下(写出最佳答案)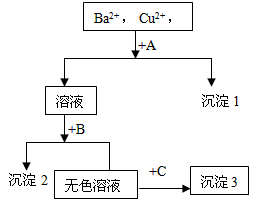
(1)写出有关物质的化学式: 试剂A __________________, 沉淀3 _________________;
(2)溶液+B的离子方程式_________________________________,
2、选择题 如果你家里的食用油混有水份,你将采用何种方法分离(? )
A过滤? ?B蒸馏
?B蒸馏
C分液? D萃取
3、选择题 下列实验方法不正确的是( )
A.用过滤的方法除去食盐水中的泥沙
B.用蒸馏的方法将自来水制成蒸馏水
C.用四氯化碳萃取碘水中的碘
D.除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶
4、实验题 碘是重要的无机化工原料,海藻灰化法是我国目前制碘的主要方法。某研究性学习小组查阅文献,设计并进行了以下模拟实验。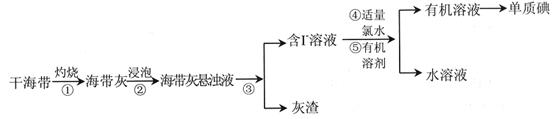
请回答:
(1)步骤①中灼烧海带用到的实验仪器是______________________(填序号)。
a. 试管? b. 坩埚? c. 烧杯
(2)步骤③的实验操作是_______________________。
(3)步骤④中反应的离子方程式是_____________________________________。
(4)步骤⑤中,可以选择的有机溶剂是__________________(填序号)。
a. 乙酸? b. 四氯化碳? c. 酒精? d. 苯
(5)同学们观察到完成步骤⑤后,所得到的水溶液呈淡黄色。某同学推断其中可能含有碘单质,检验方法是: __________________________________________________________________________。
(6)因过量的Cl2会与I2反应,所以步骤④中加入的氯水应保持适量。为证明此说法,某同学做如下实验:取少量碘水,滴加氯水,观察到碘水逐渐褪色,经检验生成物含有IO3-。该反应的化学方程式是_________________________________。
5、选择题 有关气体制备所用试剂及检验气体所用试剂不正确的组合是(?)
A.CO2;大理石和稀硫酸,;澄清石灰石;
B.Cl2;二氧化锰和浓盐酸,湿润的淀粉碘化钾试纸;
C.O2;二氧化锰和双氧水,带火星的木条;
D.NH3;氯化铵固体和氢氧化钙固体,湿润的红色石蕊试纸;