ʱ��:2020-08-13 05:57:27
1��ѡ���� ����Ԫ��R��ԭ�������ʽ������ʽ��ʾ��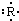
����Ԫ����ɵ��������ʣ������ʽ�϶�������ǣ�������
A�����������ʽ����ΪH3RO4
B�����������ʽ����ΪHRO3
C����̬�⻯�����ʽΪRH5
D��������������ʽΪR2O5
�ο��𰸣�Ԫ��R��ԭ�������ʽ������ʽ��ʾ��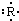
�����ݵ���ʽ��֪ԭ������������5��������ϼ�ӦΪ+5�ۣ���ͻ��ϼ�Ϊ-3�ۣ���
A������ϼ�Ϊ+5�ۣ���ΪPԪ�أ����������ʽΪH3RO4����A��ȷ��
B������ϼ�Ϊ+5�ۣ���ΪNԪ�أ����������ʽΪHRO3����B��ȷ��
C����ͻ��ϼ�Ϊ-3�ۣ�����̬�⻯�����ʽΪRH3����C����
D������ϼ�Ϊ+5�ۣ���������������ʽΪR2O5����D��ȷ��
��ѡC��
���������
�����Ѷȣ���
2������� Ԫ��A��B��Ӧ�ĵ��ʶ��ǻ�ѧ���ʱȽϻ��õ����ʣ�
��1��A�ĵ����������ǻ���ɫ���壬��Ԫ��A��Ԫ�����ڱ��е�λ����______����______�壬ʵ������ȡA���ʵ����ӷ���ʽ��______��
��2��B�ǵ��������г�ϡ������Ԫ���⣬ԭ�Ӱ뾶����Ԫ�أ���B��һ����������ɫΪ����ɫ������������к��еĻ�ѧ������Ϊ______��
�ο��𰸣���1���������ǻ���ɫ����ĵ�������������Ԫ�ص�ԭ�ӽṹʾ��ͼΪ��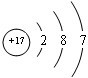
������Ӳ���=������=3��������������=��������=7�����Ը�Ԫ����Ԫ�����ڱ��д��ڵ������ڵ�VIIA�壬ʵ�����ö������̺�Ũ�����ڼ�����������ȡ��������Ӧ���ӷ���ʽΪ��MnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��
�ʴ�Ϊ��3����A��MnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��
��2��B�ǵ��������г�ϡ������Ԫ���⣬ԭ�Ӱ뾶����Ԫ�أ�ΪNaԪ�أ�����������ȼ�����ɵ���ɫ����������ƣ��������Ƶĵ���ʽΪ��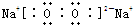
�������Ӻ���������֮��������Ӽ�����ԭ�Ӻ���ԭ��֮����ڹ��ۼ����ʴ�Ϊ�����Ӽ������ۼ���
���������
�����Ѷȣ�һ��
3������� ����������Ԫ��A��B��C��D��ԭ������������������A��Cͬ���壬B��C��Dͬ���ڣ�Aԭ�ӵ������������Ǵ�����������3����B�Ƕ�����Ԫ����ԭ�Ӱ뾶��������Ԫ�أ��Իش��������⣺
��1��A��Ԫ�ط���______��D��ԭ�ӽṹʾ��ͼ��
��2��A��B��C����Ԫ���γɵļ����ӵİ뾶�ɴ�С��˳����______��
��3��A��B��C��D�γɵĻ�����B2A2��CD2��D2A��DA2�и�ԭ�Ӷ����������8���ӽṹ����______����д����Ļ�ѧʽ?����
��4��CA2��DԪ�صĵ�����ˮ��Һ�з�Ӧ�����ӷ���ʽ��______��
�ο��𰸣�Aԭ�ӵ������������Ǵ�����������3������AΪOԪ�أ�B�Ƕ�����Ԫ����ԭ�Ӱ뾶��������Ԫ�أ���BΪNaԪ�أ�����������Ԫ��A��B��C��D��ԭ������������������A��Cͬ���壬��CΪSԪ�أ�B��C��Dͬ���ڣ���DΪClԪ�أ�
��AΪOԪ�أ�BΪNaԪ�أ�CΪSԪ�أ�DΪClԪ�أ�
��1��AΪO��Ԫ�أ�Ԫ�ط���ΪO��DΪClԪ�أ�����������Ϊ17����3�����Ӳ㣬����������Ϊ7��ԭ�ӽṹʾ��ͼΪ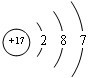
��
�ʴ�Ϊ��O��
��
��2��A��B��CԪ���γɵļ����ӷֱ���O2-��Na+��S2-��Na+��O2-���ӵĺ�������Ų���ͬ���˵����Խ�����Ӱ뾶ԽС���������Ӱ뾶O2-��Na+��S2-��O2-��������������ͬ�����Ӳ�Խ�࣬���Ӱ뾶Խ���������Ӱ뾶S2-��O2-���������Ӱ뾶S2-��O2-��Na+��
�ʴ�Ϊ��S2-��O2-��Na+��
��3��B2A2��CD2��D2A��DA2�ֱ���Na2O2��SCl2��Cl2O��ClO2����������Ϊ���ӻ������ԭ�Ӷ����������8���ӽṹ��SCl2��Cl2O��ClO2�ǹ��ۻ��������������+���ϼ۾���ֵ=8��������8���ӽṹ������SCl2��Cl2O���������8���ӽṹ��
�ʴ�Ϊ��Na2O2��SCl2��Cl2O��
��4����������ǿ�����ԣ�����Һ�н�������������Ϊ���ᣬ��Ӧ���ӷ���ʽΪSO2+Cl2+2H2O�T4H++2Cl-+SO42-��
�ʴ�Ϊ��SO2+Cl2+2H2O�T4H++2Cl-+SO42-��
���������
�����Ѷȣ�һ��
4������� ��A��B��C��D���ֶ�����Ԫ�أ����ǵ�ԭ��������A��D����������֪A��Bԭ������ͬ�ĵ��Ӳ�������A��L���������K���������������C����ȼ��ʱ���ֻ�ɫ���棬C�ĵ����ڵ�ȼʱ��������B���ʳ�ַ�Ӧ�����Եõ���D������ɫ��ͬ�ĵ���ɫ��̬������Ը������������ش�
��1��C���ӽṹʾ��ͼ��______��
��2��AB2�ĽṹʽΪ______��
��3��C2D�ĵ���ʽ��______��
��4��д����B��C��D����Ԫ����ɵ����ֻ�����Ļ�ѧʽ______��______��
�ο��𰸣���A��B��C��D���ֶ�����Ԫ�أ����ǵ�ԭ��������A��D����������֪A��Bԭ������ͬ�ĵ��Ӳ�������A��B����ͬһ���ڣ���A��L���������K�����������������A��2�����Ӳ㣬L�������Ϊ4����AΪ̼Ԫ�أ�C����ȼ��ʱ���ֻ�ɫ���棬��CΪ��Ԫ�أ�C�ĵ����ڵ�ȼʱ��������B���ʳ�ַ�Ӧ�����Եõ���D������ɫ��ͬ�ĵ���ɫ��̬�������BΪ��Ԫ�أ�DΪ��Ԫ�أ�
��1��������������Ϊ11�����������Ϊ10���������8�����ӣ������ӽṹʾ��ͼΪ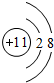
��
�ʴ�Ϊ��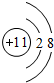
��
��2��CO2������̼ԭ������ԭ���γ�2�Թ��õ��Ӷԣ��ṹʽΪO�TC=O��
�ʴ�Ϊ��O�TC=O��
��3��C2D�����ƣ����������������ӹ��ɣ����Ƶ���ʽΪ
��
�ʴ�Ϊ��
��
��4��BΪ��Ԫ�أ�CΪ��Ԫ�أ�DΪ��Ԫ�أ���B��C��D����Ԫ����ɵ����ֻ�����Ļ�ѧʽΪNa2SO4��Na2SO3��
�ʴ�Ϊ��Na2SO4��Na2SO3��
���������
�����Ѷȣ���
5��ѡ���� ��֪X��Y��ZΪ��������Ԫ�أ��ֱ��γ�Xn+��Ym+��Zn-�������ӣ���֪m��n��X��Y������ԭ�ӵ�M���������Ϊ����������˵���в���ȷ���ǣ�������
A�����������У�Ym+���ӵİ뾶��С
B��Z������������ˮ����ķ���ʽΪHnZO4
C��X��Y��Zһ����ͬһ���ڣ���ԭ�Ӱ뾶Z��X��Y
D������Ԫ����Ӧ������������ˮ����֮����ܻ�����������Ӧ
�ο��𰸣�X��Y��ZΪ��������Ԫ�أ��ֱ��γ�Xn+��Ym+��Zn-�������ӣ���X��Y��Z����ԭ�ӵ�M���Ӳ��еĵ�������Ϊ��������X��Y��Z һ�����ڵ�3���ڣ����γɼ�����ΪXn+��Ym+��Zn-������ֵm��n������XΪ��Ԫ�أ�YΪ��Ԫ�أ�ZΪ��Ԫ�أ�
A��������������ͬ�����Ӳ�Խ�����Ӱ뾶Խ���������Ӱ뾶Cl-��Na+�����Ӳ��Ų���ͬ���˵����Խ�����Ӱ뾶ԽС�����Ӱ뾶Na+��Al3+������Al3+���Ӱ뾶��С����A��ȷ��
B��Z������������ˮ����HClO4������n=1��HClO4����HnZO4����B��ȷ��
C��ͬ����ԭ�Ӱ뾶��ԭ�����������Ӷ���С��X��Y��Z�뾶���μ�С����C����
D��X��Y��Z������������Ӧˮ����ֱ�ΪNaOH��Al��OH��3��HClO4��Al��OH��3�����������������NaOH��
HClO4��Ӧ��NaOH��HClO4����������кͷ�Ӧ����D��ȷ��
��ѡ��C��
���������
�����Ѷȣ���