时间:2020-08-13 05:56:25
1、计算题 (6分)把10.2 g镁铝合金的粉末放入过量的盐酸中,得到11.2 L H2(标准状况下)。试
计算:(原子量:Mg―24、Al―27)
(1)该合金中镁的质量分数。
(2)该合金中镁与铝的物质的量之比。
(3)该合金溶于足量的烧碱溶液中,产生H2的体积(标准状况下)是多少?
2、选择题 把含硫酸铵和硝酸铵的混合液a L分成两等份。一份加入含b mol NaOH的溶液并加热,恰好把NH3全部赶出;另一份需消耗c mol BaCl2才能使SO42-完全沉淀,则原溶液中NO3-的物质的量浓度为
A.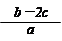
B.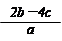
C.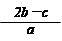
D.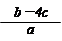
3、选择题 与3.2克SO2所含的氧原子数相等的NO质量为( )
A.6.4克
B.3.2克
C.4.6克
D.3.0克
4、计算题 某气体的分子组成是RO2,在标准状况下,1.28 g这种气体的体积是448 mL。求此气体的摩尔质量和R的相对原子质量。
5、计算题 (4分)有硫酸、硫酸铜、硫酸铁的混合溶液100mL,已知溶液中各阳离子的物质的量浓度相等,硫酸根离子的浓度为6.0mol・L-1。
(1)溶液中铜离子的物质的量为?,
(2)此溶液理论上最多可溶解铁粉的质量?。