时间:2020-08-13 05:56:25
1、填空题 (12分)天然碱是一种重要的矿物质,盛产于我国的青海湖地区。某天然碱样品的成分可以看成是碳酸钠、碳酸氢钠和水按物质的量之比1:1:2形成的结晶水合物。请回答下列问题:
(1)这种天然碱中碳酸钠、碳酸氢钠和水三者的质量比为 。
(2)45.2 g此天然碱与100 mL密度为1.1 g/cm3的中等浓度盐酸恰好完全反应,产生a mol CO2,则a= ,盐酸中溶质的质量分数ω(HCl)= %。
(3)用一个化学方程式表示该天然碱与盐酸的反应:
。
2、选择题 设NA为阿伏加德罗常数的值,下列说法中正确的是(? )。
A.2.4 g金属镁所含电子数目为0.2 NA
B.16 g CH4所含原子数目为NA
C.17 g NH3 所含质子数目为10 NA
D.18 g水所含原子数目为NA
3、选择题 用NA表示阿伏加德罗常数的值。下列叙述正确的是

 ?
?
A.25℃时,PH=13的1.0L Ba(OH)2溶液中含有的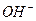 数目为0.2NA
数目为0.2NA
B.室温下,0.100 mol・L-1碳酸钠溶液中,CO32-数目小于0.2NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
4、选择题 NA代表阿伏加德罗常数,下列叙述错误的是(?)
A.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2NA个电子
B.1 mol羟基中电子数为10NA
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.常温下,1 L 0.1 mol・L-1的NH4NO3溶液中氮原子数为0.2NA
5、选择题 下列说法错误的是
A.从1L1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L
B.制成0.5L10mol/L的盐酸,需要氯化氢气体112L(标准状况)
C.0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子总物质的量为3mol
D.10g98%硫酸(密度为1.84g/cm3)与10mL18.4mol/L硫酸的浓度是不同的