ʱ��:2020-08-13 05:23:00
1��ѡ���� ���ڻ�ѧ��Ӧ��3W��g��+2X��g�� 4Y ��g��+ 3Z��g�������з�Ӧ���ʹ�ϵ�У���ȷ����?
4Y ��g��+ 3Z��g�������з�Ӧ���ʹ�ϵ�У���ȷ����?
[? ]
A��V(W)= 3V(Z)
B��2V(X) = 3V(Z)
C��2V(X) = V(Y)
D��2V(W) = 3V(X)
�ο��𰸣�CD
���������
�����Ѷȣ���
2��ѡ���� ij�¶��£����淴ӦmA(g)+nB(g) pC(g)+qD(g)ƽ�ⳣ��ΪK������˵����ȷ����(? )
pC(g)+qD(g)ƽ�ⳣ��ΪK������˵����ȷ����(? )
A��KԽ�ﵽƽ��ʱ����Ӧ���еij̶�Խ��
B��K�����¶ȵ����߶�����
C��KԽС���ﵽƽ��ʱ����Ӧ���ת����Խ��
D��K�淴Ӧ��Ũ�ȵĸı���ı�
�ο��𰸣�A
���������K��������Ƿ�Ӧ���еij̶ȣ�KֵԽ��Ӧ���еij̶�Խ��A�ԣ�ֻ������ӦΪ���ȷ�Ӧ��K�������¶ȵ����߶�������Ϊ�÷�Ӧ�����Ȼ��Ƿ��ȷ�Ӧ�������B����KֵԽ��Ӧ���ת����Խ��C����Kֻ���¶��йأ��뷴Ӧ���Ũ���أ�D����
�����Ѷȣ�һ��
3������� ����[CO��NH2��2]�����������˹��ϳɵ��л����ҵ�Ϻϳ����صķ�Ӧ���£�
2NH3(g)��CO2(g)  ?CO(NH2)2(l) �� H2O (l)?��H < 0?���ش��������⣺
?CO(NH2)2(l) �� H2O (l)?��H < 0?���ش��������⣺
��֪��ҵ�Ϻϳ����ط��������У���ط�Ӧ���£�
��Ӧ��2NH3(g)��CO2(g)  ?NH2COONH4(s)? ��H1< 0
?NH2COONH4(s)? ��H1< 0
��Ӧ��NH2COONH4(s)  ?CO(NH2)2(l)�� H2O (l)? ��H 2> 0
?CO(NH2)2(l)�� H2O (l)? ��H 2> 0
��1������ʾ��ͼ��[a��ʾ2NH3��g��+CO2��g����b��ʾNH3COONH4��s����c��ʾCO��NH2��2��l��+H2O��l��]������ȷ��ʾ���غϳɹ����������仯�����ǣ�����ţ�?��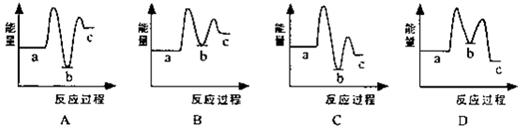
��2��ijʵ��С��ģ�ҵ�Ϻϳ����ص��������ں㶨�¶��£��������Ͷ�����̼��2��1�����ʵ���֮�ȳ���һ���Ϊ10L���ܱ������У���������������䣬�������������Բ��ƣ�����20min�ﵽƽ�⣬������Ũ�ȵı仯��������ͼ��ʾ��
��2���ٴ�ͼ�е�֪?c(CO2)=0.2mol/L,��v(CO2)= ?c(CO2)/t= 0.01mol��L-1��min-1��
�������������£��ӷ�Ӧ��ʼ��20minʱ��������̼��ƽ����Ӧ����Ϊ?��
��Ϊ������صIJ��ʣ����п��Բ�ȡ�Ĵ�ʩ��?��
A����С��Ӧ�������ݻ�
B�������¶�
C��ƽ����ϵ�м�ʱ�����CO��NH2��2
D��ʹ�ú��ʵĴ���
�۸÷�Ӧ��ƽ�ⳣ������ʽK=?����������ϵ���¶ȣ�������NH3�����������
?������ӡ�������С�����䡱����
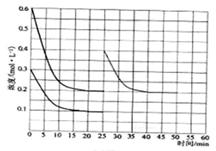
��������ƽ����¶Ⱥ�������䣬25minʱ���������г���2mol������1mol������̼����40minʱ���´ﵽƽ�⣬������ͼ�л���25~50min�ڰ�����Ũ�ȱ仯���ߡ�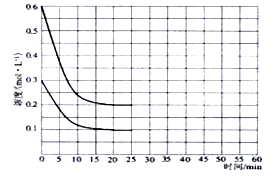
�ο��𰸣���12�֣�
��1��C
��2����0.01mol��L-1��min-1?��A
��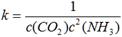 ?����
?����
��
�����������1����Ӧ���Ƿ��ȷ�Ӧ��������a>b���ܷ�Ӧ�Ƿ��ȷ�Ӧ��������a>c�����ϵ���Cͼ��
��A���С�����ƽ�������ƶ�������ȷ��B���ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ����ʴ���C�ƽ����ϵ�м�ʱ�����CO��NH2��2���ı�Һ�����ƽ�ⲻ�ƶ����ʴ���D�ƽ�ⲻ�ƶ����ʴ�����ѡA����ƽ�ⳣ�����������������Ũ����֮����ȥ��Ӧ�������Ũ����֮����
���������⿼���˻�ѧƽ��֪ʶ��������ѧƽ��Ľ����������ȣ���Ŀ�ѶȽϴ��������Ӧ��ԭ���ǽ���Ĺؼ���
�����Ѷȣ�һ��
4������� ������CuO��CO�з������·�Ӧ��CuO��s����CO��g�� Cu��s����CO2��g������֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
Cu��s����CO2��g������֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����£�
| �¶�/�� | 1 000 | 1 150 | 1 300 |
| ƽ�ⳣ�� | 4��0 | 3��7 | 3��5 |
�ο��𰸣���1�� c(CO2)��c(CO) ��?������2��0.006 mol/(L��min) ��? 60������3�� C
�����������1��ƽ�ⳣ������һ�������£����淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ�����Ը÷�Ӧ��ƽ�ⳣ������ʽK��c(CO2)��c(CO)�����ݱ������ݿ�֪�������¶�ƽ�ⳣ���Ǽ�С�ģ���˵������Ӧһ���Ƿ��ȷ�Ӧ��
��2��������CO�����ʵ�����x��������CO2��x������ƽ��ʱ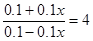 �����x��0.6mol������CO2�ķ�Ӧ������
�����x��0.6mol������CO2�ķ�Ӧ������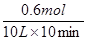 ��0.006 mol/(L��min)��CO��ƽ��ת���ʣ�0.6��1.0��0.6��
��0.006 mol/(L��min)��CO��ƽ��ת���ʣ�0.6��1.0��0.6��
��3����������Ӧ�Ƿ��ȵġ��������Ŀ��淴Ӧ�����Խ���CO2��Ũ��ƽ��������Ӧ�����ƶ���CO��ת����������ģ�ѡ��C��ȷ���ı�����������ƽ�ⲻ�ƶ���AB����ȷ�������¶�ƽ�����淴Ӧ�����ƶ���ת���ʽ��ͣ�D����ȷ�ı�ѹǿ��ʹ�ô�����ƽ�ⶼ�Dz��ƶ��ģ�������ȷ�Ĵ�ѡC��
�����Ѷȣ�һ��
5��ѡ���� ��һ�������£�ij�ܱ������з�����Ӧ��2SO2��g��+O2��g��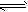 2SO3��g������H=-196.6kJ��mol-1����Ӧ��ƽ���SO2��O2��SO3�����ʵ���֮��Ϊ3��2��4�������������䣬�����¶ȣ��ﵽ�µ�ƽ��ʱ��
2SO3��g������H=-196.6kJ��mol-1����Ӧ��ƽ���SO2��O2��SO3�����ʵ���֮��Ϊ3��2��4�������������䣬�����¶ȣ��ﵽ�µ�ƽ��ʱ��
n��SO2��=1.4mol��n��O2��=0.9mol�����ʱSO3�����ʵ���Ϊ
[? ]
A��1��4mol
B��1��6mol
C��1��8mol
D��2��0mol
�ο��𰸣�A
���������
�����Ѷȣ�һ��