时间:2020-08-13 04:49:38
1、选择题 下列各反应达到化学平衡后,加压或降温都能使化学平衡向逆反应方向移动的是
A.2NO2 N2O4(正反应是放热反应)
N2O4(正反应是放热反应)
B.C(s)+CO2 2CO (正反应是吸热反应)
2CO (正反应是吸热反应)
C.N2+3H2 2NH3(正反应是放热反应)
2NH3(正反应是放热反应)
D.H2S H2+S(s)(正反应是吸热反应)
H2+S(s)(正反应是吸热反应)
2、选择题 在一定条件下,向一固定容积的容器中投入2molNO2进行反应:2NO2 2NO+O2,一段时间后测得NO2、NO、O2的物质的量可能是
2NO+O2,一段时间后测得NO2、NO、O2的物质的量可能是
[? ]
A.2?mol?NO、0.75?mol?O2?
B.1?mol?NO2、1.2?mol?NO?
C.2?mol?NO?
D.0.7?mol?O2?
3、填空题 合成气(CO+H2)是一种重要的化工原料,在化工生产中具有十分广泛的用途。?可以生产被称为21世纪的新型燃料――甲醇、二甲醚(CH3OCH3)等物质。其工艺流程如下:
(1)写出用合成气生产二甲醚的化学方程式?。 ?(2)尾气循环中涉及到以下反应:CH4(g)+H2O(g)? CO(g)+3H2(g),请写出某温度下该反应的平衡常数表达式?。
?(2)尾气循环中涉及到以下反应:CH4(g)+H2O(g)? CO(g)+3H2(g),请写出某温度下该反应的平衡常数表达式?。
(3)工业上一般采用下列两种反应合成甲醇: 反应Ⅰ: CO(g)+2H2(g)? CH3OH(g)?
反应Ⅰ: CO(g)+2H2(g)? CH3OH(g)?
 反应Ⅱ:CO2(g)+3H2(g)? CH3(g)+H2O(g)
反应Ⅱ:CO2(g)+3H2(g)? CH3(g)+H2O(g)
①下表所列数据是反应在不同温度下的化学平衡常数(K)。
| 温度 | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
 ?0(填“>”、“=”、“<”)。
?0(填“>”、“=”、“<”)。 O2(g)
O2(g) =-192.9kJ・mol-1
=-192.9kJ・mol-1 O2(g)
O2(g) =-241.8kJ・mol-1
=-241.8kJ・mol-1 =?。
=?。4、选择题 A、B两种物质当浓度恒定时,在不同温度下进行反应:A +3B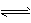 3C。10℃时,反应速率v(B) =0.3 mol.(L.s)-1; 50℃时,反应速率v(A) =25.6 mol.(L.s)-1。若该反应温度每升高10℃,化学反应速率增至n倍,则n值为
3C。10℃时,反应速率v(B) =0.3 mol.(L.s)-1; 50℃时,反应速率v(A) =25.6 mol.(L.s)-1。若该反应温度每升高10℃,化学反应速率增至n倍,则n值为
[? ]
5、填空题 (10分)一定的温度下向2L密闭容器中通入2molSO2和2molO2,发生反
应: 2SO2+O2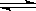 2SO3.5min后达到平衡,测得容器中有SO31.6mol.
2SO3.5min后达到平衡,测得容器中有SO31.6mol.
回答下列问题:
(1)?反应5min内,v(O2)=_________mol.L-1.min-1.
(2)?化学反应达到平衡时,SO2消耗的浓度占起始浓度的百分比为__________;此时,容器中c(O2)=_______,压强是起始时的_______倍.
(3)?判断该反应达到平衡的标志是_______________;
A.v消耗(SO2)=v生成(SO3)
B.混合气体的平均相对分子质量不再改变
C.混合气体的密度不再改变
D.容器中气体的总物质的量不再变化