时间:2020-07-28 05:26:27
1、选择题 影响一定量气体占有体积大小的主要因素是( )
A.气体分子的微粒数
B.微粒本身的大小
C.微粒的质量
D.微粒间的平均距离
参考答案:气体粒子间距离较大,远大于粒子的直径,所以粒子大小可以忽略不计,决定气体体积的因素主要为构成物质的粒子数和粒子间的距离.一定质量的气体,气体的分子数目一定,故一定温度下,影响一定质量气体体积大小的决定因素是气体分子间的平均距离,
故选D.
本题解析:
本题难度:一般
2、选择题 设NA为阿伏加德罗常数的值,下列叙述中正确的是(?)
A.标准状况下,22. 4L CO2和O2混合气体中含有的氧原子数约为NA
B.常温常压下,0. 1mol Fe在0.lmol Cl2中充分燃烧,转移的电子数为0.3NA
C.标准状况下,11. 2L NO与11. 2L O2混合后所含原子数为2NA
D.电解精炼铜时,电解池中每转移1mol电子,阳极上溶解的铜原子数为NA
参考答案:C
本题解析:略
本题难度:简单
3、选择题 设NA为阿伏加德罗常数的值,下列说法错误的是
A.6.2g白磷(P4)分子含有的P-P键数目为0.3NA
B.23.4gNa2O2固体中含有的阴离子数目为0.3 NA
C.标准状况下,2.24LNO2气体溶于水,转移的电子数为0.3 NA
D.常温常压下,4.2g乙烯和丙烯的混合气体中含有的碳原子数为0.3NA
参考答案:C
本题解析:略
本题难度:一般
4、选择题 如图:2个甲分子反应生成1个丙分子和3个乙分子,下列说法错误的是( )
A.根据阿伏加德罗定律可推知,1个乙分子中含有2个A原子
B.该反应类型是分解反应
C.反应产物均属于单质
D.此化学反应中分子的种类发生了改变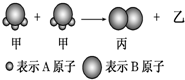
参考答案:A、根据原子守恒定律知,1个乙分子中含有2个A原子,故A错误;
B、该反应是由一种物质生成两种物质,所以属于分解反应,故B正确;
C、根据原子守恒定律知,乙的化学式可表示为A2,根据图示知,丙的化学式为B2,乙、丙都是单质,故C正确;
D、反应前是一种分子,反应后是两种分子,所以化学反应中分子的种类发生了改变,故D正确.
故选A.
本题解析:
本题难度:简单
5、选择题 设NA表示阿伏加德罗常数,下列说法不正确的是
A.甲烷的摩尔质量与NA 个甲烷分子的质量在数值上相等。
个甲烷分子的质量在数值上相等。
B.NA个氧分子和NA个氢气分子的质量比为16:1
C.28g氮气所含的原子数目为NA
D.NA个硫酸分子中所含的氧原子个数与4NA个水分子中所含氧原子个数相等
参考答案:C
本题解析:略
本题难度:简单