ʱ��:2020-07-28 05:08:30
1������� ������ʵ��д�����з�Ӧ���Ȼ�ѧ����ʽ��
��1����25�桢101kPa�£�1g�״�ȼ������CO2��Һ̬ˮʱ����22��68kJ�����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ_______________________________��
��2����������N2��O2��ȫ��Ӧ��ÿ����23g NO2��Ҫ����16��95kJ����
____________________________��
��3����֪��1mol H��H����1molN��H����1molN��N���ֱ���Ҫ��������436kJ��391kJ��946kJ����N2��H2��Ӧ����NH3���Ȼ�ѧ����ʽΪ_____________________________��
�ο��𰸣���1��CH3OH(l)+3/2O2(g)��CO2(g)+2H2O(l) ��H��-725��76kJ��mol-1
��2��N2(g)+2O2(g) === 2NO2(g) ��H��+67��8kJ��mol-1
��3��N2(g)+3H2(g) === 2NH3(g) ��H����92kJ��mol-1
���������
�����Ѷȣ�һ��
2��ѡ���� �����Ȼ�ѧ����ʽ��˵����ȷ����
[? ]
A�������ȼ����Ϊ��H=-890 kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g)=CO2(g)+
2H2O(g) ��H=-890 kJ/mol
B��500�桢30MPa�£���0.5 mol N2��1.5 mol H2�����ܱյ������г�ַ�Ӧ����NH3(g)������19.3 kJ�����Ȼ�ѧ����ʽΪ��N2(g)+3H2(g)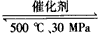 2NH3(g) ��H=-38.6 kJ/mol
2NH3(g) ��H=-38.6 kJ/mol
C����֪��H2(g)+F2(g)=2HF(g) ��H= -270 kJ/mol����1mol������1 mol������Ӧ����2 molҺ̬������ų�������С��270 kJ
D����C����ͬ�����£�2 mol HF���������С��1 mol ������1mol�����������ܺ�
�ο��𰸣�D
���������
�����Ѷȣ���
3������� ��1����֪��2SO2��g��+O2��g��?2SO3?��g����H=-196.6kJ?mol-1��2NO��g��+O2��g��?2NO2��g����H=-113.0kJ?mol-1 ����ӦNO2��g��+SO2��g��?SO3��g��+NO��g���ġ�H=______kJ?mol-1
һ�������£���NO2��SO2?�������1��2�����ܱ������з���������Ӧ��������˵����Ӧ�ﵽƽ��״̬����______��
a����ϵѹǿ���ֲ�
b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���
d��ÿ����1mol SO3��ͬʱ����1mol NO2
��2��CO�����ںϳɼ״�����Ӧ����ʽΪCO��g��+2H2��g��?CH3OH��g����CO�ڲ�ͬ�¶��µ�ƽ��ת������ѹǿ�Ĺ�ϵ��ͼ1��ʾ���÷�Ӧ��H______0���������������ʵ����������������250�桢1.3��104kPa���ң�ѡ���ѹǿ��������______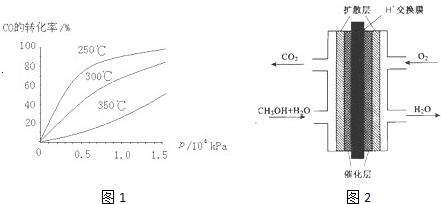
��3���״���CH3OH��ȼ�ϵ�صĽṹʾ��ͼ��ͼ2���״�����______��������������������������ĵ缫��ӦΪ______��
��4��101kPaʱ����16gCH3OH��ȫȼ������Һ̬ˮ���ų�����Ϊ363.25kJ/mol����״�ȼ�յ��Ȼ�ѧ����ʽΪ______��
�ο��𰸣���1�����ݸ�˹���ɣ����ڶ�������ʽ�ߵ����������һ������ʽ��ӵã�2NO2+2SO2�T2SO3+2NO����H=-83.6 kJ?mol-1����NO2+SO2?SO3+NO����H=-41.8 kJ?mol-1��
a������Ӧ�Ƿ�Ӧǰ���������������ķ�Ӧ������ϵ��ѹǿ���ֲ��䣬��a����˵����Ӧ�Ѵﵽƽ��״̬��
b�����ŷ�Ӧ�Ľ��У�NO2��Ũ�ȼ�С����ɫ��dz����b����˵����Ӧ�Ѵ�ƽ�⣻
c��SO3��NO�����������������1��1����c������Ϊƽ��״̬���ж����ݣ�
d��d���������������ʶ����淴Ӧ���ʣ�������Ϊƽ��״̬���ж����ݣ���ѡb��
�ʴ�Ϊ��-41.8��b��
��2����ͼ��֪���¶����ߣ�CO��ת���ʽ��ͣ�ƽ�����淴Ӧ�����ƶ������淴Ӧ�����ȷ�Ӧ������Ӧ�Ƿ��ȷ�Ӧ����H��0��ѹǿ�������ڼӿ췴Ӧ���ʣ�������ʹƽ�������ƶ�����ѹǿ������Ҫ�Ķ������豸��Ҫ��Ҳ�ߣ���ѡ��250�桢1.3��104kPa���ҵ���������Ϊ��250�桢ѹǿΪ1.3��104 kPaʱ��CO��ת�����ѽϴ�������ѹǿ��CO��ת���ʱ仯����û�б�Ҫ������ѹǿ��
�ʴ�Ϊ��������1.3��104kPa�£�CO��ת�����ѽϸߣ�������ѹǿCO��ת������߲��������ɱ����ӵò���ʧ��
��3���״�ȼ�ϵ���У��״���CԪ�صĻ��ϼ����ߣ���״�Ϊ�����������Ϊ�ᣬ�״�ʧȥ�������ɶ�����̼���缫��ӦΪCH3OH+H2O-6e-=CO2+6H+�������������ϵõ����ӷ�����ԭ��Ӧ������Һ������ˮ����Ӧ�ĵ缫��ӦΪ��O2+4H++4e-�T2H2O��
�ʴ�Ϊ������?O2+4H++4e-�T2H2O��
��4��101kPaʱ����16gCH3OH���ʵ���Ϊ0.5mol����ȫȼ������Һ̬ˮ���ų�����Ϊ363.25kJ/mol����1mol�״�ȼ�շ���726.5KJ����Ӧ���Ȼ�ѧ����ʽΪ��CH3OH��l��+3/2?O2��g���TCO2��g��+2H2O��l����H=-726.5?kJ/mol��
�ʴ�Ϊ��CH3OH��l��+3/2 O2��g���TCO2��g��+2H2O��l����H=-726.5 kJ/mol��
���������
�����Ѷȣ�һ��
4��ѡ���� �״����ӽ���Ĥȼ�ϵ���н��״�����ת��Ϊ���������ַ�Ӧԭ���ǣ�
��CH3OH(g)��H2O(g)=CO2(g)��3H2(g)�� ��H=��49��0 kJ��mol-1
��CH3OH(g)��1/2O2(g)=CO2(g)��2H2(g)������H=��192��9 kJ��mol-1����
����˵����ȷ����
[? ]
A��CH3OH�ķ�Ӧ�Ȳ���������ʵ�״̬�йأ�Ҳ��μӷ�Ӧ�ķ�Ӧ������й�
B��CH3OH������ȼ���ȴ���676��7kJ��mol-1
C��CH3OHת���H2�Ĺ���ֻ����һ���Ӹ��������������Ĺ���
D�����ݢ���֪��Ӧ��CO2(g)��3H2(g)=CH3OH(l)��H2O(g) �ġ�H����49��0kJ��mol-1
�ο��𰸣�BD
���������
�����Ѷȣ�һ��
5��ѡ���� ����ʯ�ͼ۸������ǣ�Ϊ�����ԴΣ������ʡ���ƹ�ʹ���Ҵ�������Ϊ������ȼ�ϣ����������в���һ���������Ҵ����Դ���һ�������͡���֪�Ȼ�ѧ����ʽ��1/2C2H5OH(l)+ 3/2O2(g)=CO2(g)+3/2H2O(l)��H=-683.4kJ/mol�������й�˵����ȷ����
[? ]
A.�Ҵ�������һ�������Դ��ȼ�ղ�������κ���Ⱦ
B.��25�桢101kPaʱ������1molˮʱ�ų�683.4kJ������
C.�Ҵ���ȼ����Ϊ1366.8kJ/mol
D.C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g) ��H=-1366.8kJ/mol
�ο��𰸣�C
���������
�����Ѷȣ�һ��