时间:2020-07-08 01:57:58
1、选择题 若4g CO2中含有N个分子,则阿伏加德罗常数是(?)
A.11N/3 mol-1
B.1/11N mol-1
C.11Nmol-1
D.3N/11 mol-1
参考答案:C
本题解析:CO2的摩尔质量是44g/mol,所以有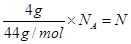 ,解得
,解得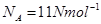 ,答案选C。
,答案选C。
本题难度:一般
2、选择题 10g?10%的氢氧化钠溶液稀释成50mL,所得氢氧化钠溶液的物质的量浓度为( )
A.0.02mol/L
B.0.05mol/L
C.0.25mol/L
D.0.5mol/L
参考答案:10g10%的氢氧化钠溶液中溶质的质量为10g×10%=1g,
则NaOH的物质的量为1g40g/mol=0.025mol,
所以氢氧化钠溶液的物质的量浓度为0.025mol0.05L=0.5mol/L,
故选D.
本题解析:
本题难度:一般
3、选择题 质量分数为90%的硫酸溶液和10%的硫酸溶液等体积混合后,溶液中溶质的质量分数(? )
A.大于50%
B.等于50%
C.小于50%
D.不能作上述比较
参考答案:A
本题解析:显然,当90%的硫酸溶液和10%的硫酸溶液以等质量混合所得溶液的质量分数为: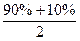 =50%
=50%
质量分数为90%的硫酸溶液和10%的硫酸溶液的密度大小关系为:90%的硫酸溶液>10%的硫酸溶液。
所以等体积(不是等质量)的这两种硫酸溶液的总质量:90%的硫酸溶液>10%的硫酸溶液,那么,混合后所得溶液的质量分数必定大于50%。
本题难度:简单
4、选择题 下列各组数值或物理量中,都不随水的“物质的量”的变化而变化的是
A.水的沸点;水分子的数目
B.水的密度;水的摩尔质量
C.水的体积;水中所含原子的数目
D.水的质量;水的相对分子质量
参考答案:B
本题解析:因水的沸点、水的密度、水的相对分子质量、水的摩尔质量都不随水的“物质的量”的变化而变化。水分子数目、水的体积、水中所含氢原子数目、水的质量均与水的“物质的量”的成正比,因此正确的答案选B。
本题难度:一般
5、选择题 在常温常压下的以下物质①10mL水②100mL氯气③220mL氖④120mL二氧化碳,这四种物质中所含原子数由多到少的顺序是?
A.①②③④
B.①④③②
C.③④②①
D.④③②①
参考答案:B
本题解析: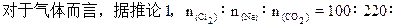
120,原子数之比:100×2∶220∶120×3=200∶220∶360。所以三者由多到少顺序为④③②,①中水为液态,其物质的量远远大于其余三种,故B项符合题意。
本题难度:一般