时间:2020-07-08 01:39:39
1、填空题 已知短周期的主族元素X、Y、Z、W、M的原子序数依次增大,X是空气中含量最
多的元素,其单质的化学性质非常稳定,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W元素形成的单质为淡黄色的固体,M元素形成的单质为黄绿色气体.请回答以下问题:
(1)X元素的符号是????,它在周期表的位置为??;
(2)Z的氧化物晶体类型为??,化学式是:??;
(3)X与Y能形成离子化合物,该化合物的电子式为?;
(4)X的最高价氧化物的水化物与Y的氧化物反应的化学方程式为??;
(5)X、W形成的氢化物分别为甲和乙,且甲、乙所含的电子数相等,则甲的结构式为?;
(6)W和M都是较活泼的非金属元素,用实验事实表明这两种元素的非金属性强弱(用方程式书写或文字说明)?。
参考答案:(1)N,第二周期第ⅤA族(2)原子晶体 ,SiO2
(3)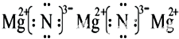
(4)2HNO3+MgO=Mg(NO3)2+2H2O?
(5)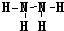 ?
?
(6)Cl2+H2S=2HCl+S,
本题解析:X是空气中含量最多的元素,X为氮元素;Z单质可制成半导体材料,Z为硅元素;则Y是镁元素;W元素形成的单质为淡黄色的固体,M元素形成的单质为黄绿色气体,则W、M为硫、氯。
(1)X元素符号是N,是第三周期第ⅤA族元素;
(2)Z的氧化物是SiO2,属于原子晶体;
(3)X与Y形成的离子化合物为Mg3N2电子式为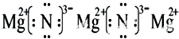
(4)X的最高价氧化物的水化物是HNO3,Y的氧化物是MgO,二者反应的化学方程式为2HNO3+MgO=Mg(NO3)2+2H20;
(5)X、W形成的氢化物分别为甲和乙,且甲、乙所含的电子数相等,甲为N2H4,乙为H2S, N2H4的结构式为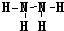 ;
;
(6)S的非金属性比Cl的弱,可用Cl2和H2S反应置换S。
本题难度:一般
2、选择题 下列各组的几种分子中所有原子都可能处于同一平面的是
A.CH4、CS2、BF3
B.CO2、H2O、NH3
C.C2H4、C2H2、C6H6
D.CCl4、BeCl2、PH3
参考答案:C
本题解析:A项中的CH4,C是sp3杂化,正四面体构型,所有原子不可能处于同一平面,B项中的NH3,N是sp3杂化,三角锥构型,所有原子不可能处于同一平面,D项中的CCl4,C是C是sp3杂化,正四面体构型,所有原子不可能处于同一平面。答案选C。
点评:sp3杂化正四面体构型,sp2杂化平面三角形,sp杂化直线型。
本题难度:一般
3、选择题 下列物质中既含有离子键又含有极性共价键、非极性共价键的是( )
A.H2O2
B.CaCl2
C.Na2CO3
D.CH3CH2ONa
参考答案:D
本题解析:
本题难度:简单
4、填空题 元素周期表中第四周期元素由于受3d电子的影响,性质的递变规律与短周期元素略有不同。
Ⅰ.第四周期元素的第一电离能随原子序数的增大,总趋势是逐渐增大的。
镓(31Ga)的基态电子排布式是_________________________________________;
31Ga的第一电离能却明显低于30Zn,原因是______________________________________;
Ⅱ.第四周期过渡元素的明显特征是形成多种多样的配合物。
(1)CO和NH3可以和很多过渡金属形成配合物。CO与N2互为等电子体,CO分子中C原子上有一孤电子对,C、O原子都符合8电子稳定结构,则CO的结构式可表示为________________。NH3 分子中N原子的杂化方式为_______杂化,NH3分子的空间立体构型是____________。
(2)向盛有硫酸铜水溶液的试管中加氨水,首先形成蓝色沉淀,继续加入氨水沉淀溶解,得到深蓝色透明溶液,向该溶液中加乙醇,析出深蓝色晶体。蓝色沉淀先溶解,后析出的原因是:__________________________________________(用相关的离子方程式和简单的文字说明加以解释)
(3)如图甲所示为二维平面晶体示意图,所表示的化学式为AX3的是________。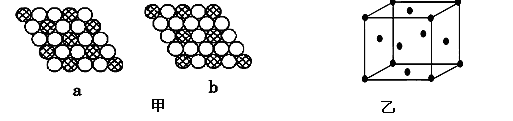
(4)图乙为一个金属铜的晶胞,此晶胞立方体的边长为acm,Cu的相对原子质量为64,金属铜的密度
为ρ g/cm3,则阿伏加德罗常数可表示为________ mol-1(用含a、ρ的代数式表示)。
参考答案:Ⅰ、31Ga的电子排布式是:1s22s22p63s23d104s24p1? (2分)?
30Zn的4s能级处于全充满状态,较稳定?(2分)
Ⅱ、(1)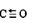 (只写三键没标明配位键的只给1分)(2分) SP3 (1分)?三角锥型(1分)
(只写三键没标明配位键的只给1分)(2分) SP3 (1分)?三角锥型(1分)
(2)蓝色沉淀与氨水可发生如下反应:Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++4H2O+2OH-,
生成的[Cu(NH3)4]SO4在极性较小的乙醇中溶解度较小而析出。(3分)
(方程式正确给2分,其它回答正确也可得3分)
(3)b(2分)
(4)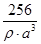 mol-1 ?(2分)
mol-1 ?(2分)
本题解析:Ⅰ、 31Ga的电子排布式是:1s22s22p63s23d104s24p130Zn的4s能级处于全充满状态,较
稳定Ⅱ(1)CO分子中碳和氧共用两对电子,氧提供一对电子配位;NH3是以氮原子为中心,三个氢
原子和氮的一对孤对电子,以sp3不等性杂化方式形成三角锥型
(2) 蓝色沉淀与氨水可发生如下反应:Cu(OH)2+4NH3?H2O=[Cu(NH3)4]2++4H2O+2OH-,生成的[Cu(NH3)4]SO4在极性较小的乙醇中溶解度较小而析出。
(3)a图中一个黑的周围有6个相邻白点,一个白的周围有3个相邻黑点,黑:白=1:2
b图中一个黑的周围有6个相邻白点,一个白的周围有2个相邻黑点,黑:白=1:3故选b
(4)金属铜的晶胞为面心立方晶胞,含有6个面心,8个顶点,每个面心是两个晶胞所共用,顶点是8个晶胞所共用,平均每个晶胞中铜原子的个数为6×(1/2)+8×(1/8)=4,每个晶胞4个Cu原子。1mol 的Cu原子质量为64g,1mol的晶胞Cu原子质量就是4X64g
晶胞体积×晶胞密度×阿佛加德罗常数="4×64g" 计算可知:阿佛加德罗常数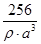 mol-1
mol-1
本题难度:一般
5、选择题 下列物质中,既含有离子键又含有极性共价键的是?
[? ]
A.NaOH?
B.NaCl?
C.N2?
D.H2O
参考答案:A
本题解析:
本题难度:简单