时间:2020-07-08 01:28:26
1、选择题 下列说法正确的是(NA表示阿伏加德罗常数)( )
A.在常温常压下,11.2LN2含有的分子数为0.5NA
B.在常温常压下,1molHe含有的原子数为NA
C.71gCl2所含原子数为2NA
D.23g钠在化学反应中失去电子数目为10NA
参考答案:A.常温常压下,Vm≠22.4L/mol,11.2LN2的物质的量不等于0.5mol,故A错误;
B.He为单原子分子,则1molHe含有的原子数为NA,故B正确;
C.n(Cl2)=1mol,Cl2为双原子分子,则71gCl2所含原子数为2NA,故C正确;
D.Na原子核外有1个电子,23g钠在化学反应中失去电子数目为NA,故D错误.
故选BC.
本题解析:
本题难度:简单
2、选择题 下列说法正确的是(NA表示阿伏加德罗常数)
A.在常温常压下,11.2L?CH4含有的分子数为0.5NA
B.常温常压下,0.5mol氦气含有的原子数为NA
C.32g氧气所含电子数目为16NA
D.同温同压下,相同体积的任何气体单质所含的原子数目都为NA
参考答案:C
本题解析:分析:A、气体摩尔体积22.4L/mol必须使用于标况下的气体;
B、结合氦气是单原子分子分析计算;
C、质量换算物质的量,结合一个氧气分子中含有电子数为16分析计算;
D、根据分子分为单原子分子和多原子分子;
解答:A、CH4含有的分子数N=nNA= NA,由于不是标况,气体摩尔体积22.4L/mol不能代入,故A错误;
NA,由于不是标况,气体摩尔体积22.4L/mol不能代入,故A错误;
B、一个氦气中含有一个原子,所以0.5?mol氦气含有的原子数为0.5?NA,故B错误;
C、32g氧气的物质的量为1mol,所以32g氧气所含电子数目为16NA,故C正确;
D、同温同压下,相同体积的任何气体单质的物质的量相等,分子的数目相等,但分子分为单原子分子和多原子分子,故D错误;
故选:C.
点评:阿伏伽德罗常数考查知识面覆盖广,具有很好的区分度,是历年高考倍受青睐的试题,问题解决重在审题,并且善于总结常见易错点.
本题难度:简单
3、选择题 用NA表示阿伏加德罗常数的数值,则下列说法中正确的是( )
A.常温常压下,18gH2O所含质子数为10NA
B.常温常压下,11.2L氧气含原子数为NA
C.2.3g金属钠变为钠离子得到0.1NA电子
D.常温常压下,NA个氢分子的质量为1g
参考答案:A、1molH2O分子含质子数10mol,18gH2O为1mol,含质子数为10NA,故A正确;
B、常温常压下,11.2L氧气的物质的量不是0.5mol,所以含原子数不是NA,故B错误;
C、2.3g金属钠变为钠离子失去0.1NA电子,故C错误;
D、常温常压下,NA个氢分子为1mol,氢气的质量为2g?mol-1×1mol=2g,故D错误;
故选A.
本题解析:
本题难度:简单
4、选择题 两个体积相同的密闭容器一个盛有氯化氢,另一个盛有H2和Cl2的混合气体,在同温同压下,两个容器内的气体一定具有相同的
A.质量
B.密度
C.电子总数
D.原子总数
参考答案:D
本题解析:根据阿伏伽德罗定律,同温同压下的气体体积相同,物质的量相同。则两容器中气体的物质的量相同,因为均为双原子分子,所以具有相同的原子总数。
考点:阿伏伽德罗定律。
本题难度:一般
5、选择题 设NA为阿伏加德罗常数的值,下列有关叙述不正确的是
A.标准状况下,1L甲烷完全燃烧所生成的气态产物的分子数为NA
B.1?mol甲基(-CH3)所含的电子总数为7NA
C.0.5?mol?1,3-丁二烯分子中含有C=C双键数为?NA
D.1?mol碳正离子(CH)所含的电子总数为8NA
参考答案:B
本题解析:分析:A、标准状况下,1L甲烷的物质的量是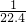 mol,完全燃烧生成二氧化碳
mol,完全燃烧生成二氧化碳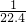 mol;
mol;
B、甲基没有得失电子,1mol甲基中含有9mol电子;
C、1mol1,3-丁二烯分子中含有2mol碳碳双键,0.5mol分子中含有1mol碳碳双键;
D、碳正离子中含有8个电子,1 mol碳正离子(CH )含有8mol电子.
)含有8mol电子.
解答:A、标况下,1L甲烷的物质的量是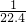 mol,完全燃烧生成气体二氧化碳
mol,完全燃烧生成气体二氧化碳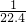 mol,气态产物的分子数为
mol,气态产物的分子数为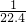 NA,故A错误;
NA,故A错误;
B、由于甲基没有得失电子,1mol甲基中含有9mol电子,所含的电子总数为9NA,故B正确;
C、由于1mol1,3-丁二烯分子中含有2mol碳碳双键,0.5mol分子中含有1mol碳碳双键,含有C=C双键数为NA,故C错误;
D、由于碳正离子中含有8个电子,1 mol碳正离子(CH )含有8mol电子,所含的电子总数为8NA,故D错误;
)含有8mol电子,所含的电子总数为8NA,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数,注意甲基没有得失电子,碳正离子有电子的转移,本题难度不大.
本题难度:一般