时间:2020-07-08 01:18:57
1、选择题 把500mL含有氯化钡和氯化钾的混合溶液分成5等份,取一份加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀,另取一份加入含bmol硝酸银的溶液,恰好使氯离子完全沉淀,则该混合溶液中钾禽子浓度为(? )
A.10(b-2a)mol/L
B.10 (b-a)mol/L
C.10(2a-a)mol/L
D.0.1(b-2a)mol/L
2、选择题 用1L?1mol?L-1NaOH溶液吸收0.9molCO2,所得溶液中的CO32-和HCO3-的物质的量浓度之比是( )
A.5:4
B.4:5
C.1:8
D.8:1
3、选择题 某气体物质质量为6.4 g,含有6.02×1022个分子,则该气体的相对分子质量为(? )
A.64
B.32
C.96
D.16
4、实验题 某同学帮助水质检测站配制480 mL 0.5 mol・L-1NaOH溶液以备使用。
(1)该同学应选择 mL的容量瓶。
(2)其操作步骤如乙图所示,则甲图操作应在乙图中的 (填选项字母)之间。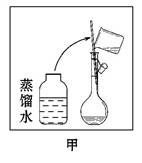
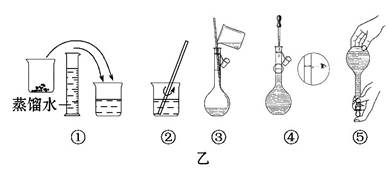
A.②与③ B.①与② C.③与④
(3)该同学应称取NaOH固体 g,用质量为23.1 g的烧杯放在托盘天平上称取所需NaOH固体时,请在附表中选取所需的砝码大小 (填字母),并在下图中选出能正确表示游码位置的选项 (填字母)。
附表 砝码规格
| | a | b | c | d | e |
| 砝码大小/g | 100 | 50 | 20 | 10 | 5 |
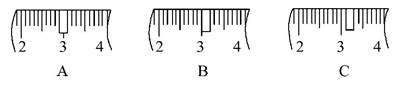
5、选择题 科学家不久前制得一种新型分子O4。2 mol O4和4 mol O2 含有的
A.电子数相同,分子数不同
B.质量相同,电子数不同
C.原子数相同,质子数不同
D.分子数相同,质量不同