时间:2020-07-08 01:02:29
1、填空题 (6分)设水的电离平衡线如右图所示。 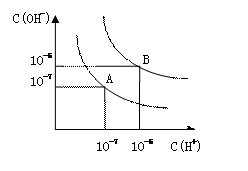
(1)若以A点表示25℃时水在电离平衡时的粒子浓度,当温
度升高到100℃时,水的电离平衡状态到B点,则此时水的离子
积从___________增加到____________; A
(2)将PH=8的Ba(OH)2溶液与PH=5的稀盐酸混合,并保持
在100℃的恒温,欲使混合溶液的PH=7,则Ba(OH)2溶液和盐
酸的体积比为__________。
参考答案:(1)10-14 10-12 (2)2:9
本题解析:略
本题难度:一般
2、选择题 HA和HB两种酸的溶液分别加水稀释时,pH变化的简图如图所示,下列叙述中不正确的是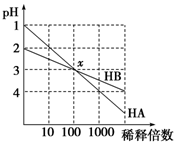
A.HA是一种强酸
B.x点,[A-]=[B-]
C.HB是一种弱酸
D.原溶液中HA的物质的量浓度为HB的10倍
参考答案:D
本题解析:A、根据图像可知HA稀释前pH=1,稀释100倍后pH=3,这说明在稀释过程中氢离子的物质的量不变,因此HA是强酸,A正确;B、x点两种溶液的pH相等,则根据电荷守恒可知[H+]=[OH-]+[A-]、[H+]=[OH-]+[B-],所以x点,[A-]=[B-],B正确;C、稀释前HB的pH=2,稀释100后pH=3,这说明在稀释过程中溶液中氢离子的物质的量是增加的,因此溶液中存在电离平衡,所以HB是弱酸,C正确;D、稀释前HA的浓度是0.1mol/L。但由于HB是弱酸,不能确定HB的浓度,所以无法计算原溶液中HA的物质的量浓度与HB的物质的量浓度关系,D不正确,答案选D。
本题难度:一般
3、选择题 pH="2" 的两弱酸HA.HB加水稀释后,溶液 pH随加水量的变化曲线如图所示。则下列叙述正确的是:(?)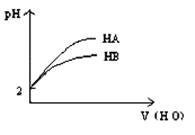
A.电离平衡常数HA > HB
B.等体积等pH的HA 和HB与等浓度的NaOH反应,HA消耗的NaOH多
C.等体积等pH的HA和HB 与等质量的Zn反应,HA反应速率大
D.若有等浓度的NaA.NaB,则碱性NaA>NaB
参考答案:A
本题解析:依据图示可知,两种酸都是弱酸,稀释过程中HA的PH变化比HB大,说明酸性HA大于HB;A.由于酸性HA>HB,故电离平衡常数HA>HB,A正确;B.酸性HA>HB,等PH时,HA的浓度一定小于HB的,由等体积,HA的物质的量一定小于HB的物质的量,HB消耗的氢氧化钠多,B错误;C.等体积等pH的HA和HB 与等质量的Zn反应,酸性HA>HB,浓度HA<HB,反应前溶液中氢离子浓度相等,反应中氢离子浓度HB的变化小,故与锌反应,开始时速率相等,之后HB的反应速率大,C错误;D.对应的酸的酸性越弱,水解程度越大,酸性HA>HB,故水解程度NaA<NaB,则碱性NaA<NaB,D错误;故选A.
本题难度:一般
4、填空题 (4分)有H+浓度相同、体积相等的三种酸:a、盐酸? b、硫酸? c、醋酸,同
时加入足量的锌,则开始时反应速率由大到小的顺序是?(用
a、b、c表示), 完全反应后生成H2的体积由大到小是 ??。
参考答案:a=b=c?a=b<c
本题解析:盐酸是一元强酸,硫酸是二元强酸,醋酸是一元弱酸,则在氢离子浓度相同的条件下,和锌反应时最初的反应速率是相等的。由于醋酸的浓度最大,所以醋酸产生的氢气最多,而盐酸和硫酸产生的氢气是相等的。
点评:该题是高考中的常见题型,属于中等难度的试题,试题基础性强,侧重对学生解题方法的培养和训练,有利于培养学生的逻辑思维能力和抽象思维能力,提高学生的灵活应变能力。
本题难度:一般
5、选择题 已知某温度下,几种酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol・L-1、Ka(HF)= 6.8×10-4 mol・L-1、Ka(CH3COOH)= 1.8×10-5 mol・L-1、、Ka(HNO2)= 6.4×10-6mol・L-1。则物质的量浓度都为0.1 mol・L-1的下列溶液中,pH最小的是
A.NaCN
B.NaF
C.CH3COONa
D.NaNO2
参考答案:B
本题解析::相同的浓度,酸的电离常数越大,说明其酸性越强,由题干可以知道Ka(HCN)= 6.2×10-10 mol・L-1、Ka(HF)= 6.8×10-4 mol・L-1、Ka(CH3COOH)= 1.8×10-5 mol・L-1、、Ka(HNO2)= 6.4×10-6mol・L-1,HF的电离常数最大,所以其酸性最强,所以其盐的水解程度较小,即pH最小,所以本题的答案为B。
点评:本题考查了酸的电离常数,盐类水解,这些知识点是高考考查的重点和难点,本题难度不大。
本题难度:一般