时间:2020-07-08 01:01:26
1、实验题 某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下: 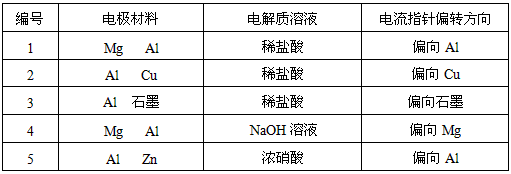
试根据上表中的实验现象回答下列问题:
(1)实验1、2中Al所作的电极是否相同?____________。
(2)写出实验3中的电极反应式。
铝为( )_____________________________________;
石墨为( )___________________________________;
(3)实验4中的铝作正极还是负极?写出电池总反应方程式。
________________________________________
(4)解释实验5中电流指针偏向铝的原因。
________________________________________
(5)根据实验结果总结:在原电池中金属铝作正极还是作负极受哪些因素的影响?
________________________________________
参考答案:
(1)不同
(2)负极;2Al-6e-==2Al3+;正极;6H++6e-==3H2↑
(3)负极;电池总反应式:2Al+2NaOH+6H2O==2Na[Al(OH)4]+3H2↑
(4)由于铝在浓硝酸中发生钝化,反以锌为负极
(5)与另一种材料的活泼性、电解质溶液的酸碱性以及电解质溶液的氧化性强弱等因素有关
本题解析:
本题难度:困难
2、简答题 将HCl、H2SO4、Ba(NO3)2三种溶液,按一定顺序依次滴入到Na2CO3溶液中至恰好完全反应,并有以下现象:①滴加A时生成白色沉淀②再滴加B时沉淀溶解,并有气体逸出③往生成的溶液中加入C时,又有白色沉淀生成.根据上述现象,回答:
(1)A、B、C各是什么溶液(填写溶质的化学式)A______B______C______
(2)写出上述反应的离子方程式
①______;
②______;
③______.
参考答案:①能和碳酸钠反应生成白色沉淀的是硝酸钡;②再滴加B时沉淀溶解,并有气体逸出,则B为盐酸;因硫酸能和钡离子反应生成硫酸钡白色沉淀,③往生成的溶液中加入C时,又有白色沉淀生成,则C为硫酸,
(1)通过以上分析知,A是 Ba(NO3)2 B是HCl,C是硫酸.故答案为:Ba(NO3)2;HCl;H2SO4;
(2)①钡离子和碳酸根离子反应生成碳酸钡白色沉淀,离子方程式为Ba2++CO32-=BaCO3↓,故答案为:Ba2++CO32-=BaCO3↓;
②碳酸钡和盐酸反应生成钡离子、二氧化碳和水,离子方程式为BaCO3+2H+=Ba2++CO2↑+H2O,故答案为:BaCO3+2H+=Ba2++CO2↑+H2O;
③钡离子和硫酸根离子反应生成硫酸钡白色沉淀,离子方程式为:Ba2++SO42-=BaSO4↓,故答案为:Ba2++SO42-=BaSO4↓.
本题解析:
本题难度:一般
3、实验题 工业上常用铁质容器盛装冷浓酸。为研究铁质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(1)将已去除表面氧化物的铁钉(碳素钢)放入冷浓硫酸中,10分钟后移人硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是____________。
(2)另称取铁钉6.0g放入15.0ml.浓硫酸中加热,充分应后得到溶液X并收集到气体Y。 ①甲同学认为X中除 外还可能含有
外还可能含有 ?。若要确认其中的
?。若要确认其中的 ?,应选用_____________。
?,应选用_____________。
a.KSCN溶液和氯水?b.铁粉和KSCN溶液?c.浓氨水?d.酸性 溶液
溶液
②乙同学取336ml(标准状况)气体Y通入足量溴水中,发生反应: ?
?
然后加入足量 溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中
溶液,经适当操作后得干燥固体2.33g。由于此推知气体Y中 的体积分数为____________。
的体积分数为____________。
分析上述实验中 体积分数的结果,丙同学认为气体Y中还可能含量有
体积分数的结果,丙同学认为气体Y中还可能含量有 和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。?
和Q气体。为此设计了下列探究实验状置(图中夹持仪器省略)。? 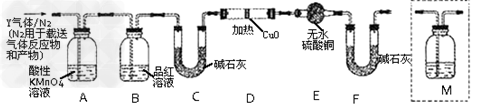
(3)装置B中试剂的作用是_____________。
(4)认为?气体Y中还含有Q的理由是____________(用化学方程式表示)。
(5)为确认Q的存在,需在装置中添加M于___________?(选填序号)。 ?
?a.?A之前?b.A-B间?c.B-C间?d.C-D间
(6)如果气体Y中含有 ?,预计实验现象应是______________。
?,预计实验现象应是______________。
(7)若要测定限定体积气体Y中 ?的含量(标准状况下约有
?的含量(标准状况下约有 28ml?),除可用测量
28ml?),除可用测量 体积的方法外,可否选用质量称量的方法?做出判断并说明理由____________________.
体积的方法外,可否选用质量称量的方法?做出判断并说明理由____________________.
参考答案:(1)铁钉表面被钝化
(2)①d?②66.7%
(3)检验 是否除尽
是否除尽
(4) ?
?
(5)c
(6)D中固体由黑变红和E中固体由白变蓝
(7)否,用托盘天平无法称量D或E的差量
本题解析:
本题难度:困难
4、简答题 有机物间的反应很复杂,往往有很多副反应发生;如乙醇与浓硫酸的混合溶液在不同温度下发生的反应类型不同,再如卤代烃(CaHbX,X指代Cl、Br、I等)在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物;因此在有机化学学习中知道各种有机反应的类型和对应反应发生所需条件是非常重要的.试回答下列问题:
(1)结合目前所学,试总结有机物在浓硫酸加热条件下可发生有机反应的类型有______;
(2)卤代烃①在NaOH水溶液加热条件下发生的反应类型是取代反应,②在NaOH醇溶液加热条件下发生的反应类型是消去反应.现要证明某卤代烃(CaHbX,X指代Cl、Br、I等)中存在何种卤素,你选择上述两条件中的哪一条(填序号)?并说明你这样选的理由:______.
(3)为证明溴乙烷在NaOH乙醇溶液中发生的是消去反应,在你设计的实验方案中,需要检验的是______,检验的方法是______(需说明:所用的试剂、简单的实验操作及预测产生的实验现象).
参考答案:(1)有机物在浓硫酸加热条件下可发生有机反应有,苯的硝化反应,磺化反应,乙醇的消去反应、分子间脱水反应、酯化反应等,
故答案为:取代(酯化、硝化)反应、消去反应;
(2)检验卤代烃中的卤素元素的存在,需要先把卤代烃水解,使卤原子变化为卤素离子,选择①,因为不是所有的卤代烃都能发生消去反应,
故答案为:选择①,因为所有的卤代烃都能在该条件下水解,而只有与卤素原子相连的碳的邻碳上有氢的卤代烃才能在NaOH醇溶液加热条件下发生反应;
(3)验证卤代烃溴乙烷在强碱的醇溶液中发生消去反应,生成乙烯、溴化钠和水,和卤代烃在强碱的水溶液中加热生成物比较可知,都含有溴化钠,所以需要验证乙烯的存在,利用乙烯的加成反应,乙烯通入溴水中 褪色证明发生的是消去反应,
故答案为:乙烯的存在;将溴乙烷在NaOH乙醇溶液中共热产生的气体通入盛有溴水的试管,若溴水褪色,则说明发生了消去反应.
本题解析:
本题难度:一般
5、实验题 谷氨酸一钠盐是味精的主要成分,谷氨酸一钠盐在水溶液中存在如下平衡:
⑴当前我国生产味精主要采用淀粉发酵法,其中第一步是使淀粉水解为单糖。实验室中检验淀粉水解产物可选用的试剂是?。
A.NaOH溶液、氨水、AgNO3溶液
B.H2SO4溶液、氨水、AgNO3溶液
C.NaOH溶液、CuSO4溶液
D.H2SO4溶液、CuSO4溶液
⑵“沙伦逊甲醛滴定法”可用于测定味精中谷氨酸一钠盐的含量。其方法如下:
将一定质量的味精样品溶于水,再向溶液中加入36%甲醛溶液,发生的反应如下:
R―NH2+HCHO→R―N=CH2+H2O(R表示除“-NH2”外的基团),再以酚酞为指示剂,用NaOH溶液进行滴定。
①上述测定过程中加入甲醛的目的是?。
②滴定终点的实验现象为?。
⑶味精中常含食盐,有两个同学分别设计甲、乙两种方案来测定味精中NaCl的含量。
①甲方案:取一定质量味精样品溶于水,加入足量稀硝酸酸化的硝酸银溶液,充分反应后,?(填写操作步骤),称量沉淀质量。
②乙方案:取mg味精溶于水,加入过量浓度为c1mol・L―1的AgNO3溶液,再加入少量?溶液做指示剂,用浓度为c2mol・L―1的NH4SCN溶液进行滴定,当溶液变为红色时,达到滴定终点。已知:AgSCN是难溶于水的沉淀。
设测定过程中所消耗的AgNO3溶液和NH4SCN溶液的体积分别为V1mL和V2mL,则该味精样品中NaCl的质量分数是?。
参考答案:⑴AC?⑵①掩蔽氨基,避免氨基影响羧基和NaOH的中和反应
②溶液由无色变为红色(且半分钟不褪色)?⑶①过滤、洗涤、干燥
②Fe(NO3)3?
本题解析:(1)淀粉的水解产物是葡萄糖,葡萄糖中含有醛基,可被新制的氢氧化铜悬浊液或银氨溶液氧化,所以答案选AC。
(2)①由于氨基显碱性,所以为了防止氨基干扰羧基和NaOH的中和反应,可用甲醛掩蔽氨基。
②酚酞能使碱显红色,所以终点时的现象是溶液由无色变为红色(且半分钟不褪色)。
(3)①氯化银不溶于水,过滤后洗涤、干燥即可。
②由于铁离子能和NH4SCN反应使溶液显红色,所以可用Fe(NO3)3作指示剂。根据题意可知,和硝酸银反应的NH4SCN是0.001V2c2mol,所以和氯化钠反应的硝酸银是0.001V1c1mol-0.001V2c2mol,所以氯化钠的物质的量是0.001V1c1mol-0.001V2c2mol,因此该味精样品中NaCl的质量分数是 。
。
本题难度:一般