时间:2020-07-08 00:59:21
1、选择题 下列说法正确的是( )
A.在标准状况下,11.2L某气体的质量为22g,则该气体的相对分子质量是44g/mol
B.16gO2和16gO3含的氧原子个数一样多
C.在标准状况下,水、氧气和氮气分子间的平均距离都相等
D.1mol氯化钙溶于水配成1L溶液,所得溶液中Cl-的物质的量浓度为1mol/L
2、选择题 下列物质中含氧原子最多的是 (相对原子质量 H—1? O—16? S—32)
A.0.2mol H2O
B.3.01×1023个SO2分子
C.49g H2SO4
D.标准状态下11.2L的O3
3、实验题 (14分)I.实验室用Na2CO3·10H2O晶体配制50 g质量分数为21.2%的Na2CO3溶液。回答下列问题:
(1)应用托盘天平称取Na2CO3·10H2O晶体??g。
(2)用托盘天平和小烧杯称出碳酸钠晶体的质量,天平平衡后的状态如下图。由图中可以看出,该同学在操作时犯了一个错误是?。实际称量的碳酸钠晶体质量为?g。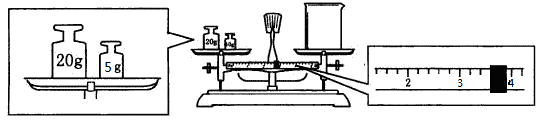
II. 实验室要配制2.5 mol/L 的稀硫酸溶液90 mL,回答下列问题:
(1)用量筒量取质量分数为98%,密度为1.84 g/cm3的浓硫酸?mL。
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒外,还缺少的仪器是?。
(3)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是?。
A.量取浓硫酸时,仰视读数
B.洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
C.稀释硫酸时,有溶液溅到桌面上
D.没有洗涤稀释硫酸的烧杯和玻璃棒
E.定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
F.容量瓶不干燥
(4)从容量瓶中取该溶液40 mL,与5 mol/L的NaOH溶液?mL恰好完全反应,反应后溶液中的c(Na+)=?(忽略溶液混合过程中的体积变化)
4、选择题 由CO2、H2和CO组成的混合气在同温同压下与氮气的密度相同.则该混合气体中CO2、H2和CO的体积比可能为(?)
A.29∶8∶13
B.22∶1∶14
C.13∶8∶29
D.29∶16∶57
5、选择题 已知某饱和溶液的①溶液的质量?②溶剂质量?③溶液体积?④溶质的摩尔质量?⑤溶质的溶解度?⑥溶液的密度。利用以上部分已知条件不可计算该溶液物质的量浓度的是(? )
A.①②④⑥
B.④⑤⑥
C.②③④⑤
D.①③④⑥