时间:2020-07-08 00:59:21
1、选择题 下列说法正确的是
A.摩尔是七个基本物理量之一
B.氮气的摩尔质量是28g
C.0.5mol氢气的体积为11.2L
D.1molH2O约含有6.02×1023个水分子
参考答案:D
本题解析:摩尔只是一个单位不是物理量,A错;摩尔质量的单位是g/mol,B错;没有“在标准状况下”这个条件无法计算气体的体积,C错,选D。
考点:常见物理量的单位和有关物质的量的计算。
本题难度:一般
2、选择题 相同状况下,下列气体所占体积最大的是
A.3g H2
B.16g O2
C.32g H2S
D.80g SO3
参考答案:A
本题解析:略
本题难度:一般
3、选择题 下列溶液中溶质的物质的量浓度是1mol/L的是
A.将40g NaOH溶解于1L水中
B.将22.4LHCl气体溶于水中配成1L溶液
C.将1L 10mol/L 的浓盐酸与9L水混合
D.将10g NaOH溶于水中配成250mL溶液
参考答案:D
本题解析: 1mol/L表示1升的溶液中所含溶质的物质的量为1mol。所以答案选D
考点:考查物质的量浓度的相关知识点。
本题难度:一般
4、选择题 在Al2(SO4)3、MgSO4、K2SO4的混合溶液中,含有的Al3+、Mg2+、SO42-的个数比是2:3:8,则溶液中Al2(SO4)3、MgSO4、K2SO4的物质的量之比是( )
A.1:2:4
B.2:3:2
C.1:2:3
D.1:3:2
参考答案:溶液呈电中性,则阴阳离子所带电荷相等,设K+的个数与Al3+、Mg2+、SO42-的个数比是x:2:3:8,则x+2×3+3×2=2×8,所以x=4,同一溶液中离子的个数之比等于其浓度之比,再根据其化学式知Al2(SO4)3、MgSO4、K2SO4的物质的量浓度之比为22:3:42=1:3:2,同一溶液中各物质的物质的量之比等于其物质的量浓度之比,
故选D.
本题解析:
本题难度:简单
5、填空题 (10分)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g/mol。若阿伏加德罗常数的值用NA表示,则:
(1)该气体的物质的量为________mol。
(2)该气体所含原子总数为_______ _个。
(3)该气体在标准状况下的体积为____________L。
(4)该气体溶于1L水中(不考虑反应),形成的溶液溶质的质量分数为 。
(5)该气体溶于水形成VL溶液,其溶液的物质的量浓度为 mol/L。
参考答案:(每空2分,共10分)
(1)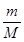
 (2)
(2)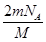 (3)
(3)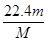
(4)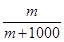 (5)
(5)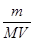
本题解析: 考(1)根据n=m/M得该气体的物质的量是m/Mmol;
(2)根据N=nNA,得该气体中所含的原子总数是m/M×NA×2=2mNA/M;
(3)根据V=Vm×n,得该气体的体积=22.4×m/M=22.4m/ML;
(4)该气体溶于1L水中得到的溶液的质量是1000+m,所以溶液中溶质的质量分数是m/(1000+m) ×100%;
(5)根据C=n/V得溶液的物质的量浓度=m/M/V=m/MVmol/L。
考点:考查物质的量、物质的量浓度、粒子数、气体体积、溶液中溶质的质量分数的计算
本题难度:一般