ʱ��:2020-07-08 00:56:53
1������� A��B��C��D��E��F��G��H����I������ѧ��ѧ�г��������壬���Ǿ��ɶ�����Ԫ����ɣ������������ʣ�
��A��I�����������̣�
��A��B��E��F��G��ʹʪ�����ɫʯ����ֽ��죬I��ʹʪ��ĺ�ɫʯ����ֽ������C��D��H����ʹʪ���ʯ����ֽ��ɫ��
��B��E����ʹƷ����Һ��ɫ��
�ܽ����ȵ�ͭ˿����װ��B��ƿ�У�ƿ�ڳ����ػ�ɫ���̣�
��Mg������F�о���ȼ�գ��к�ɫ�Ͱ�ɫ���ֲ��
��C��D�������ɺ���ɫ���壻
��G��D��ȼ�տ��Բ���E��H2O��
�ཫB��H?��ƿ�л�Ϻ����������ü����ӣ�ƿ�ڳ�����״Һ�β�����A��
�ش��������⣺
��1��A�Ļ�ѧʽ��______�����а��̵ĵ���ʽ��______��
��2�����з�����Ӧ�Ļ�ѧ����ʽ��______��
��3�����з�����Ӧ�Ļ�ѧ����ʽ��______��
��4��C�Ļ�ѧʽ��______��D�Ļ�ѧʽ��______��
��5�����з�����Ӧ�Ļ�ѧ����ʽ��______��
��6��H�Ļ�ѧʽ��______��
�ο��𰸣���A��I�����������̣�ΪNH3��HCl��
��A��B��E��F��G��ʹʪ�����ɫʯ����ֽ��죬Ϊ�������壬I��ʹʪ��ĺ�ɫʯ����ֽ������Ϊ�������壬��AΪHCl��BΪNH3��C��D��H����ʹʪ���ʯ����ֽ��ɫ������������ԣ�
��B��E����ʹƷ����Һ��ɫ��ΪCl2��SO2��
�ܽ����ȵ�ͭ˿����װ��B��ƿ�У�ƿ�ڳ����ػ�ɫ���̣���BΪCl2��EΪSO2��
��Mg������F�о���ȼ�գ��к�ɫ�Ͱ�ɫ���ֲ��FΪCO2��
��C��D�������ɺ���ɫ���壬ΪNO��O2��
��G��D��ȼ�տ��Բ���E��H2O��EΪSO2����DΪO2����CΪNO��G����H��S����Ԫ�أ�GΪH2S��
��BΪCl2����H��ƿ�л�Ϻ����������ü����ӣ�ƿ�ڳ�����״Һ�β�����A��HCl������HΪCH4�ȣ�
��1��������������֪��A�Ļ�ѧʽ��HCl���������ɵİ������Ȼ�泥���笠������������ӹ��ɣ�����ʽΪ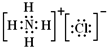
���ʴ�Ϊ��HCl��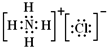
��
��2�����з����ķ�Ӧ��ͭ��������Ӧ�����Ȼ�ͭ����Ӧ����ʽΪ��Cu+Cl2?��ȼ?.?CuCl2��
�ʴ�Ϊ��Cu+Cl2?��ȼ?.?CuCl2��
��3�����з����ķ�Ӧ��Mg�ڶ�����̼��ȼ������̼Խ����þ����Ӧ����ʽΪ��2Mg+CO2?��ȼ?.?2MgO+C��
�ʴ�Ϊ��2Mg+CO2?��ȼ?.?2MgO+C��
��4�����������ӿ�֪��C�Ļ�ѧʽ��NO��D�Ļ�ѧʽ��O2���ʴ�Ϊ��NO��O2��
��5�����з����ķ�Ӧ������ȼ�����ɶ���������ˮ����Ӧ����ʽΪ��2H2S+3O2?��ȼ?.?2SO2+2H2O��
�ʴ�Ϊ��2H2S+3O2?��ȼ?.?2SO2+2H2O��
��6��������������֪��H�Ļ�ѧʽ��CH4�ȣ��ʴ�Ϊ��CH4�ȣ�
���������
�����Ѷȣ�һ��
2������� ��ͼ���漰�����ʾ�Ϊ��ѧ��ѧ�еij������ʣ�����C��DΪ���嵥�ʣ�E��Ŀǰ����Ӧ����㷺�Ľ���������Ϊ��������Ǵ�����ͼת����ϵ����Ӧ�����ɵ�ˮ����Ҫ���������ȥ��
��1��д����ѧʽ��B______��G______��
��2��ָ��MnO2����ط�Ӧ�е����ã�
��Ӧ������______������Ӧ������______����
��3�����F��B?������Ӧ�Ļ�ѧ����ʽ______
��4������Ӧ�����ڼ��������½��У�A��______��
����Ӧ�����ڳ��������½��У�A��______��
�����������������µõ�������C���ʣ���Ӧ��ת�Ƶĵ�����֮��Ϊ______��
�ο��𰸣���MnO2��Ӧ���Ʊ���������O2��Cl2�������ڲ����������£���H2O2��MnO2�Ʊ�O2���ڼ�����������Ũ�����MnO2�Ʊ�
Cl2����AΪH2O2��BΪHCl��CΪO2��DΪCl2��FΪ��������������ᷴӦ���������Ȼ���Ҷ���֮������ת����˵��EΪ��۽�����ӦΪFe����Ŀǰ����Ӧ����㷺�Ľ�������FΪFe3O4��GΪFeCl2��HΪFeCl3����
��1�������Ϸ�����֪��BΪHCl��GΪFeCl2���ʴ�Ϊ��HCl��FeCl2��
��2���ڲ����������£���H2O2��MnO2�Ʊ�O2��H2O2���������ã��ڼ�����������Ũ�����MnO2�Ʊ�Cl2��������
4HCl��Ũ��+MnO2?��?.?MnCl2+Cl2��+2H2O��MnO2�������������ã�
�ʴ�Ϊ������������
��3��Fe3O4�к���+2�ۺ�+3��Fe�����ᷴӦ����FeCl3��FeCl2����Ӧ�Ļ�ѧ����ʽΪFe3O4+8HCl=2FeCl3+FeCl2+4H2O��
�ʴ�Ϊ��Fe3O4+8HCl=2FeCl3+FeCl2+4H2O��
��4�����ݻ��ϼ۱仯�жϣ���֪��2KClO3?MnO2?.��2KCl+3O2��������3molת��12mol���ӣ�2H2O2?MnO2?.?2H2O+O2��������3molת��6mol���ӣ����ɵ����ʵ�����O2����Ӧ��ת�Ƶĵ�����֮��Ϊ2��1��
�ʴ�Ϊ��KClO3��H2O2��2��1��
���������
�����Ѷȣ�һ��
3������� ��֪���ס����ǵ��ʣ���Ϊ����ɫ���壬�������Ƶõĵ��Դ�Ѵ���Ӧ���ڵ�·�㳡�������ͺ���ƣ�B��C��D��E��F���ֻ��������ɫ��Ӧ��Ϊ��ɫ����Dת��ΪC��Eʱ����������֧��ȼ�յ���ɫ���嵥�ʣ�F�������г����ĵ�ζƷ������������һ�������´�����ͼת����ϵ�������ַ�Ӧ�������������ȥ��
��ش��������⣺
��1��B���ʵ�������______��C���ʵĻ�ѧʽΪ______��
��2��д��D����E�����ӷ�Ӧ����ʽ��______��
��3��д��B��E����Һ�з�Ӧ�����ӷ���ʽ��______��
��4����C��Һ��ͨ��ף����Ƶ�ij�������������г��õ�Ư�ס����������ʣ�ͬʱ��B���ɣ��÷�Ӧ�Ļ�ѧ����ʽ�ǣ�______��
��5��A��C��Һ��Ӧ������B���䷴Ӧ����Ϊ______��
�ο��𰸣��ס����ǵ��ʣ���Ϊ����ɫ���壬ӦΪCl2���������Ƶõĵ��Դ�Ѵ���Ӧ���ڵ�·�㳡�������ͺ���ƣ�ӦΪNa��B��C��D��E��F���ֻ��������ɫ��Ӧ��Ϊ��ɫ��˵��������NaԪ�أ���Dת��ΪC��Eʱ����������֧��ȼ�յ���ɫ���嵥�ʣ��������ΪO2����֪DӦΪNa2O2��C��EΪNaOH��Na2CO3����B��������C��֪CӦΪNa2CO3��EΪNaOH��BΪNaHCO3��F�������г����ĵ�ζƷ��ӦΪNaCl��A������NaHCO3��NaCl����������Cl2����AӦΪHCl��
��1�������Ϸ�����֪BΪNaHCO3���׳�С�մ�CΪNa2CO3���ʴ�Ϊ��С�մ�Na2CO3��
��2��Na2O2����NaOH�����ӷ�Ӧ����ʽ2Na2O2+2H2O=4Na++4OH-+O2�����ʴ�Ϊ��2Na2O2+2H2O=4Na++4OH-+O2����
��3��NaHCO3��NaOH����Һ�з�Ӧ�����ӷ���ʽΪHCO3-+OH-=CO32-+H2O���ʴ�Ϊ��HCO3-+OH-=CO32-+H2O��
��4����Na2CO3��Һ��ͨ��Cl2�����Ƶ�ij�������������г��õ�Ư�ס����������ʣ�ӦΪNaClO��ͬʱ��NaHCO3���ɣ�
�÷�Ӧ�Ļ�ѧ����ʽ��2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3��
�ʴ�Ϊ��2Na2CO3+Cl2+H2O=NaClO+NaCl+2NaHCO3��
��5��HCl��Na2CO3��Һ��Ӧ������NaHCO3����Ӧ�ķ���ʽΪNa2CO3+HCl=NaCl+NaHCO3���䷴Ӧ����Ϊ���ֽⷴӦ��
�ʴ�Ϊ�����ֽⷴӦ��
���������
�����Ѷȣ�һ��
4������� ��8�֣���֪����M��X��Y���ֶ�����Ԫ����ͬ����Ԫ����ɣ�Xԭ�ӵ����������������ڲ��������1/2 ��YԪ��������������ĸ��۴�����Ϊ6��M�����������ʵ�ת����ϵ���£����ֲ�������ȥ����
��1����A��X��Yͬ����Ԫ�ص�һ�ֵ��ʣ���F��ˮ��Һ����ʱ��GΪ�������Σ���F��ˮ��Һ����ʱ��GΪ��������E�����F��Һ��Ӧ�����ӷ���ʽ
��???��
��2����A��һ�ֳ�������������ҿ��������첣������A��B��Ӧ�Ļ�ѧ����ʽ��?��
��3����A��һ����Һ��ֻ���ܺ���H+��NH4+��Mg2+��Fe3+��A13+��CO32-��SO42-�е�ijЩ���ӣ��������Һ�м���B��Һʱ���������ɳ��������ʵ�����B��Һ������仯��ͼ��ʾ���ɴ˿�֪������Һ�п϶����е���������?���Ҹ������ӵ����ʵ���֮��Ϊ?��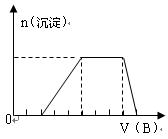
�ο��𰸣�
��1��[Al(OH)4]�D +4H+=A13++4H2O��2�֣�
��2��SiO2+2NaOH=Na?2?SiO3+H2O��2�֣�
��3��H+��NH4+��A13+?��2�֣�? 2��3��1?��2�֣�������ǰ������˳��Ӧһ�£�
�����������
�����Ѷȣ���
5������� ��ͼ�Dz��ֻ�ѧ������������͵��ʵ�ת����ϵ�����С�������f��������ά����Ҫԭ�ϣ�������c��һ�־��д��Եĺ�ɫ���ʡ��ش��������⣺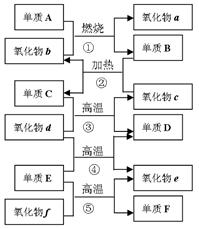
��1��д���������ʵĻ�ѧʽ������C?��������d?��
��2�������ĵ���F�ڹ�ҵ�ϵ���ҪӦ����?��
��3��д�����з�Ӧ�Ļ�ѧ����ʽ��
��?��
��?��
��?��
�ο��𰸣���1�� C��Fe�� d��H2O?������1�֣�?��2�����뵼����ϣ��缯�ɵ�·��ȣ���
��3���� 2Mg+CO2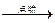 2MgO+C��?��C+ H2O
2MgO+C��?��C+ H2O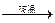 CO+H2
CO+H2
�� SiO2+2C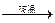 Si+2CO������2�֣�
Si+2CO������2�֣�
�����������
�����Ѷȣ���