ʱ��:2020-07-08 00:51:16
1���ƶ��� A��B��C��D��Ϊ4�ֳ����Ķ�����Ԫ�أ�ԭ��������������A��C����ɷ���ʽΪA2C2��A2C���ֳ����Ļ���������ڳ����¶� ��Һ�壻B��A�ȿ��γɷ���X��Ҳ���γ�������Y��X��Y����10���ӵ����ӣ�D ��ͬ������ԭ�Ӱ뾶���
(1)DԪ�������ڱ��е�λ����____��D�ĵ�����C�ĵ�����ȼ�����ɹ���W�ĵ���ʽΪ____�� Һ̬X����A2C��Ҳ���������Ҳ�����������ͬ���������ӣ���Һ̬X���뷽��ʽΪ____��
(2)��C�ĵ���ͨ��1 mol/L KI��0.1 mol/L H2SO4�����Һ�У���Ӧ�����ӷ���ʽΪ____��
(3)M��N�ֱ�����A��B��C��D����Ԫ���е���������Ԫ����ɵ�ǿ����ʡ�M ��ˮ��Һ�ʼ��ԣ���������ˮ�ĵ��룻N��ˮ��Һ�����ԣ����ܴٽ�ˮ�ĵ��롣��M��N�ֱ�Ϊ___��____���ѧʽ��������0.1 mol/L��M ��0.2 mol/L��N����Һ�������ϣ�������Һ������Ũ�ȵĴ�С˳��Ϊ____��
2��ѡ���� ���и���Һ�У������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�������
A��0.1mol?L-1Na2CO3��Һ�У�[OH-]=[HCO3]+[H+]��[C
3��ѡ���� ����������һ����ȷ����
[? ]
A��0.1mol/L��CH3COOH��Һ�У���ˮ�����c(H+)Ϊ10��13?mol/L?
B��pH=2��pH=1��CH3COOH��Һ��c(H+)֮��Ϊ1�U10?
C��������Na+��H+��OH����CH3COO���������ӵ�ij��Һ�п��ܴ��ڣ�c(Na+)��c(CH3COO��)��c(H+)��c(OH��)
D��1.0?mol/LNa2CO3��Һ��c(OH��)��c(HCO3��)+c(H+)+2c(H2CO3)
4��ѡ���� ���и���Һ�У��������ʵ���Ũ�ȹ�ϵ��ȷ����
[? ? ]
5��ѡ���� ��ͼΪ��������0.1000?mol/L?NaOH��Һ�ζ�20.00?mL0.1000?mol/L�����20.00?mL?0.1000?mol/L��������ߡ�����HA��ʾ�ᣬ�����жϺ�˵����ȷ����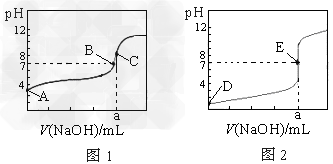
[? ]
A��ͼ1�ǵζ����������
B��B��E״̬ʱ������Һ������Ũ�Ⱦ�Ϊc(Na+)?=?c(A-)
C��C��E״̬ʱ����Ӧ���ĵ���n(CH3COOH)?=?n(HCl)?
D����0?mL<V(NaOH)<20.?00?mLʱ����Ӧ��Һ�и�����Ũ�ȴ�С˳��һ����Ϊc(A��)?>c(Na+)>?c(H+)?>?c(OH��)