时间:2020-07-08 00:30:05
1、选择题 F2和Xe在一定条件下可以生成XeF2、XeF4和XeF6三种氟化氙,它们都是极强的氧化剂(其氧化性依次递增),都极易水解,其中:6XeF4+12H2O = 2XeO3+4Xe↑+24HF +3O2↑。下列推测正确的是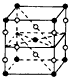
[? ]
A.XeF2分子中各原子均达到8电子稳定结构
B.某种氟化氙的晶体结构单元如上图,可推知其化学式为XeF6
C.XeF4按已知方式水解,每生成4 molXe,转移16 mol电子
D.XeF2加入水中,在水分子作用下将重新生成Xe和F2
参考答案:C
本题解析:
本题难度:一般
2、选择题 下面有关金属的叙述正确的是
A.金属原子只有还原性而其阳离子只有氧化性
B.金属阳离子只存于化合物中且有相应的阴离子相配合
C.金属单质在常温下均为金属晶体
D.某单质具有延展性则它一定是金属
参考答案:B
本题解析:A选项中若遇到二价铁离子,还具有还原性;B选项正确;C选项汞单质为液体;D选项非金属材料也具有延展性。
点评:本题的做法是举反例来对选项的内容进行判断,如果能举出反例则选项的内容是错误的。
本题难度:一般
3、填空题 (8分).C70分子是形如椭球状的多面体,该结构的建立基于以下考虑: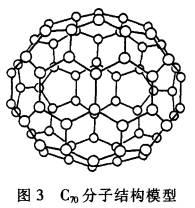
(1)C70分子中每个碳原子只跟相邻的3个碳原子形成化学键;
(2)C70分子中只含有五边形和六边形;
(3)多面体的顶点数、面数和棱边数的关系遵循欧拉定理:顶点数+面数-棱边数=2。
根据以上所述确定:
(1)C70分子中所含的单键数和双键数;(2)C70分子中的五边形和六边形各有多少?
参考答案:(1)单键数:70;双键数:35。
(2)设C70分子中五边形数为x个,六边形数为y个。
依题意可得方程组:
1/2(5x+6y)=1/2(3×70)(键数,即棱边数)
70+(x+y)-1/2(3×70)=2(欧拉定理)
解得五边形数x=12,六边形数y=25。
本题解析:略
本题难度:简单
4、选择题 纳米材料表面微粒的比例极大,这是它有许多特殊性质的原因。假设某氯化钠纳米颗粒的大小和形状恰好与氯化钠晶胞的大小和形状相同(如图所示),则这种纳米颗粒的表面微粒数与总微粒数的比值为 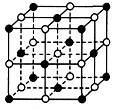
[? ]
A.7:8
B.13:14
C.25:26
D.26:27
参考答案:D
本题解析:
本题难度:一般
5、填空题 (6分)下列七种晶体:
A.二氧化硅
B.乙烷晶体
C.碳酸钠
D.氯化钠 E.晶体氩F.过氧化氢 G.镁(用字母填空)
(1)由原子直接构成的分子晶体是__________。
(2)含有非极性键的分子晶体是____________,含有离子键、共价键的化合物是___________。
(3)在一定条件下能导电且导电时未发生化学反应的是______________,受热熔化需克服共价键的是__________________,受热熔化后化学键不发生变化的是__________。
参考答案:(6分) (1)E? (2)BF? C? (3) G? A? BF(每空1分,不全对不给分)
本题解析:分子晶体有:B、E和F;原子晶体有:A;离子晶体包括C、D;金属晶体包括:G
(1)氩是单原子分子,分子之间由范德华作用力,选E
(2)乙烷CH3CH3中含有C―C非极性键,过氧化氢H2O2中含有O―O非极性键,均为分子晶体;
只要含有离子键,必属于离子离子晶体,碳酸钠阴离子中含有非金属原子之间的共价键,选C
(3)金属导电时不发生化学反应,故选镁符合条件
原子晶体受热熔化时需要克服共价键,选二氧化硅符合题意
受热熔化后化学键不发生变化的是分子晶体,故乙烷、过氧化氢符合题意
本题难度:简单