时间:2020-07-08 00:28:40
1、选择题 下列物质中,属于弱电解质的是
A.CH3COOH
B.H2SO4
C.NaOH
D.Na2CO3
参考答案:A
本题解析:乙酸是弱酸,是弱电解质。
本题难度:一般
2、选择题 已知25℃时,弱电解质的电离平衡常数:Ka(CH3COOH)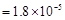 ,Ka(HSCN)
,Ka(HSCN)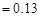 。在物质的量浓度均为
。在物质的量浓度均为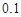 mol・L
mol・L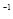 的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
的CH3COONa和NaSCN混合溶液中,下列排序正确的是( )
A.c(OH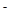 )>c(CH3COOH)>c(HSCN)>c(H
)>c(CH3COOH)>c(HSCN)>c(H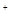 )
)
B.c(OH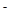 )>c(HSCN)>c(CH3COOH)>c(H
)>c(HSCN)>c(CH3COOH)>c(H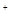 )
)
C.c(OH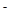 )>c(SCN
)>c(SCN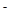 )>c(CH3COO
)>c(CH3COO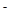 )>c(H
)>c(H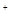 )
)
D.c(OH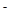 )>c(CH3COO
)>c(CH3COO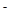 )>c(SCN
)>c(SCN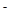 )>c(H
)>c(H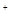 )
)
参考答案:A
本题解析:电离平衡常数越大,酸性越强。说明醋酸的酸性弱于HSCN的。但酸越弱,相应的钠盐越容易水解,碱性就越强。所以选项A正确,答案选A。
本题难度:一般
3、填空题 (12分)已知氢氟酸、醋酸、氢氰酸(HCN)、碳酸在室温下的电离常数分别为:
| ① | HF | Ka=6.8×10-4 mol?L-1 |
| ② | CH3COOH | Ka=1.7×10-5 mol?L-1 |
| ③ | HCN | Ka=6.2×10-10 mol?L-1 |
| ④ | H2CO3 | Ka1=4.4×10-7mol?L-1 Ka2=4.7×10-11 mol?L-1 |
参考答案:(1)氢氟酸,? HCN?
(2)H2CO3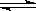 HCO3―+H+,? HCO3―
HCO3―+H+,? HCO3―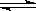 CO32―+H+
CO32―+H+
( 3)2HF+Na2CO3=2NaF+H2O+CO2↑,? NaCN+H2O+CO2= HCN+NaHCO3
本题解析:(1)电离常数越大,相应酸的酸性越强,所以根据电离常数可知,酸性最强的是氢氟酸,而最弱的是HCN。
(2)碳酸是二元弱酸,电离是分步进行的,所以电离方程式依次是
H2CO3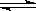 HCO3―+H+、HCO3―
HCO3―+H+、HCO3―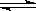 CO32―+H+。
CO32―+H+。
(3)由于氢氟酸的电离常数大于碳酸的电离常数,所以根据较强酸制取较弱的酸可知,反应的方程式是2HF+Na2CO3=2NaF+H2O+CO2↑;由于碳酸的第一步电离常数大于HCN的,但第二步小于HCN的,所以足量的CO2通入NaCN溶液中反应方程式是NaCN+H2O+CO2= HCN+NaHCO3。
本题难度:一般
4、选择题 向0.1 mol・L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度随加入氨水的体积(V)变化的曲线关系是下图中的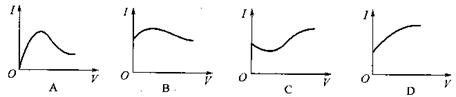
参考答案:B
本题解析:醋酸和氨水是弱电解质存在电离平衡,但溶液的导电性不可能为0。二者反应后生成的醋酸铵是强电解质,因此溶液的导电性增强。完全反应后继续加入氨水溶液的导电性开始降低,所以图像B符合,答案选B。
本题难度:简单
5、选择题 分别在[H+]=1×10-1摩/升的酸溶液和[OH-]=1摩/升NaOH溶液中加入足量的铝,放出H2的量前者多,其原因可能是?
A.两种溶液的体积相同,酸是多元强酸
B.两种溶液的体积相同,酸是弱酸
C.酸溶液的体积比NaOH溶液的体积大
D.酸是强酸,且酸溶液浓度比NaOH溶液的浓度大
参考答案:B、C
本题解析:在酸和强碱溶液中,[H+]<[OH-],若为强酸,则放出H2的量不可能比碱多,若使酸放出的气体比碱多,则酸为弱酸,使酸的浓度比碱大,可不断电离产生H+,与Al反应放出的H2量大;酸的体积比碱的体积大,酸的物质的量也可超过碱,也能达到目的。
本题难度:一般