时间:2020-07-08 00:25:47
1、选择题 要从BaCl2、NaCl的混合液中分别得到纯净的BaCl2和NaCl晶体,在一系列的操作中,应选用的试剂是
[? ]
A.碳酸钾、盐酸
B.碳酸钠、盐酸
C.碳酸钠、硫酸
D.氢氧化钠、盐酸
参考答案:B
本题解析:
本题难度:一般
2、填空题 (9分)除去下列物质中的少量杂质(括号内杂质),填写所需试剂及相关反应的离子方程式:
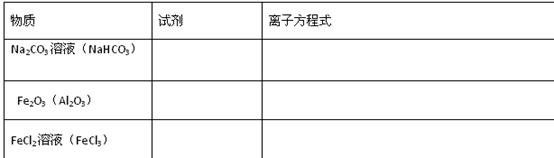
参考答案: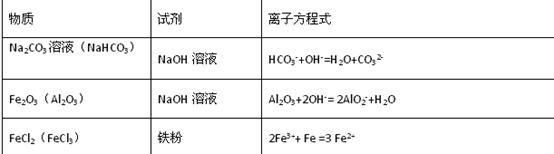
本题解析:略
本题难度:简单
3、选择题 除去下列物质中少量杂质的方法正确的是?
A.除去CO2中混有的HCl:用饱和碳酸钠溶液洗气
B.除去KCl溶液中混有的K2SO4:加入过量BaCl2溶液,过滤
C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
D.除去NaHCO3中混有的Na2CO3:用加热法
参考答案:C
本题解析:A、饱和碳酸钠溶液能与二氧化碳反应生成碳酸氢钠,将原物质除掉,不符合除杂原则,故A错误;B、用氯化钡除去氯化钾中的硫酸钾,会带入新的杂质氯化钡,能除去杂质但引入了新的杂质氯化钡,不符合除杂原则,故B错误;C、铁粉不与氯化亚铁反应,能与氯化铁反应生成氯化亚铁,故C正确;D、NaHCO3受热分解为Na2CO3,原物质被除去,故D错误。
本题难度:一般
4、简答题 为除去粗盐中的Ca2+、Mg2+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):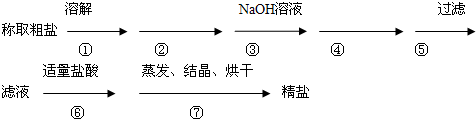
(1)步骤②中应加入的试剂是______溶液,判断此试剂已加过量的方法是______.
(2)步骤④中应加入的试剂是______溶液,第④步中相关的离子方程式是______.
(3)若将第⑤步和第⑥步颠倒,会对实验结果产生影响,其原因是______
(4)②③④中所加试剂的顺序也可以调整为______
A ③②④B?④③②C?②④③D?④②③
参考答案:(1)粗盐中的CaCl2、MgCl2、FeCl3、Na2SO4以及泥沙等杂质的除杂方法:先将混合物溶解,后过滤除泥沙,再加入试剂分别将钙离子、镁离子、铁离子以及钙离子除去,但是碳酸钠一定放在氯化钡的后面,氢氧化钠和氯化钡的顺序无要求,在粗盐提纯时,加入过量的氯化钡的目的是除去硫酸根离子,并将之除尽,氯化钡过量时,加入硫酸会产生白色沉淀,可以通过检验钡离子来确定氯化钡是否过量,所以取所得溶液的上层清液1~2滴于滴定板上,再滴入1~2滴BaCl2溶液,若溶液未变浑浊,表明BaCl2已过量,
故答案为:BaCl2;取少量上层澄清液于试管中,滴加氯化钡溶液,不再产生白色沉淀,证明氯化钡溶液已滴加过量.?或取少量上层澄清液于试管中,滴加稀硫酸,产生白色沉淀,证明氯化钡溶液已滴加过量;
(2)加入试剂碳酸钠来将溶液中的杂质离子钙离子以及多余的钡离子除去,反应方程式为:Ca2++CO32-=CaCO3↓、
Ba2++CO32-=BaCO3↓;
故答案为:Na2CO3;Ca2++CO32-=CaCO3↓、Ba2++CO32-=BaCO3↓;
(3)不能先加盐酸再过滤,如果这样会将产生的沉淀氢氧化镁、氢氧化铁以及碳酸钙溶于盐酸中,影响氯化钠的纯度,故答案为:会使CaCO3、BaCO3、Mg(OH)2沉淀溶解,重新引入Ca2+、Ba2+、Mg2+;
(4)粗盐中的CaCl2、MgCl2、FeCl3、Na2SO4以及泥沙等杂质的除杂方法:先将混合物溶解,后过滤除泥沙,再加入试剂分别将钙离子、镁离子、铁离子以及钙离子除去,但是碳酸钠一定放在氯化钡的后面,氢氧化钠和氯化钡的顺序无要求,故选A.
本题解析:
本题难度:一般
5、选择题 离子检验的常用三种方法:
A.CO32- ――气体法
B.SO42-――沉淀法
C.H+――显色法
D.Cl- ――气体法
参考答案:D
本题解析:试题分析:检验碳酸根离子的方法:向溶液中加入过量盐酸,产生无色无味使澄清石灰水变浑的气体;检验硫酸根离子的方法:向溶液中先加盐酸,无现象,再加氯化钡溶液,产生白色沉淀;检验氢离子的方法:向溶液中滴加紫色石蕊试液,溶液变红;检验氯离子的方法:向溶液中加硝酸银溶液和稀硝酸,产生白色沉淀,D错误。
考点:离子的检验
点评:检验碳酸根离子的方法可能有碳酸氢根离子的干扰。
本题难度:简单