ʱ��:2020-07-08 00:03:00
1������� ���г�����������A��B��C�ͳ�������ס��ҡ���������D��E��F��G��H������֮���ܷ������·�Ӧ��ͼ����Щ��Ӧ�IJ���ͷ�Ӧ������û��ȫ��������� ?
?
�����������Ϣ�ش��������⣺
��1��д���������ʵĻ�ѧʽ�� A?����?
��2��д����Ӧ�ڵĻ�ѧ����ʽ?
��3��д�����з�Ӧ���ӷ���ʽ��
��Ӧ��?
��Ӧ��?
��Ӧ��?
�ο��𰸣���1��Na? HCl
��2��H2+Cl2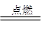 2HCl
2HCl
��3����Ӧ�ۣ�2Al��2H2O��2OH����2AlO2����3H2��
��Ӧ�ݣ�2Fe2��+ Cl2=?2Fe3�� ��2Cl��?��Ӧ�ޣ�Fe3��+ 3OH��=?Fe(OH)3��
�����������������A����ɫ��ӦΪ��ɫ��ӦΪNa����ˮ��Ӧ���ɵ������ΪH2��DΪNaOH������ɫ������ΪCl2�����ΪHCl��EΪ���ᣬ����NaOH��Ӧ����������BΪAl�����ɫ����HΪFe��OH��3����CΪFe��FΪFeCl2?��GΪFeCl3����1�������Ϸ�����֪AΪNa����ΪHCl�ʴ�Ϊ��Na��HCl��2����Ӧ��ΪH2+Cl2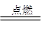 2HCl��3����Ӧ�۵Ļ�ѧ����ʽΪ��2Al+2NaOH +2H2O==2NaAlO2 + 3H2�������ӷ���ʽΪ��2Al+2H2O+2OH��==2AlO2��+3H2������Ӧ��ΪFeCl2��Cl2�ķ�Ӧ������ʽΪ2FeCl2+Cl2�T2FeCl3�����ӷ���ʽΪ��2Fe2++Cl2="2" Fe3++2Cl-?��Ӧ����ΪFeCl3��NaOH�ķ�Ӧ������ʽΪFeCl3+3NaOH�TFe��OH��3��+3NaCl�����ӷ���ʽΪ��Fe3+ +3OH-�TFe��OH��3����
2HCl��3����Ӧ�۵Ļ�ѧ����ʽΪ��2Al+2NaOH +2H2O==2NaAlO2 + 3H2�������ӷ���ʽΪ��2Al+2H2O+2OH��==2AlO2��+3H2������Ӧ��ΪFeCl2��Cl2�ķ�Ӧ������ʽΪ2FeCl2+Cl2�T2FeCl3�����ӷ���ʽΪ��2Fe2++Cl2="2" Fe3++2Cl-?��Ӧ����ΪFeCl3��NaOH�ķ�Ӧ������ʽΪFeCl3+3NaOH�TFe��OH��3��+3NaCl�����ӷ���ʽΪ��Fe3+ +3OH-�TFe��OH��3����
�����Ѷȣ�һ��
2������� ��֪A��F����ѧ��ѧ�г������ʣ�����A��C��E��FΪ���壬B��DΪҺ�壬D������������Ϊһ�����ҹ�ҵ����ˮƽ��һ�ֱ�־��F��Ũ��Һ��X����ͨ������ʵ�����Ʊ�����C��X��һ�ֺ�ɫ��ĩ��B��������18�����ӣ���Ӧ�в�������������ȥ��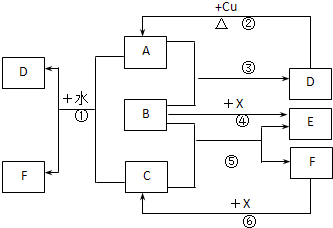
�Իش��������⣺
��1������ͼ����Ϣ������B��C��X�����Դ�ǿ������˳����______�����û�ѧʽ��ʾ��
��2��B�ĵ���ʽΪ______��������______���壮
��3��д����Ӧ�ڵĻ�ѧ����ʽ��______��
��4��д����Ӧ�١������ӷ���ʽ��
��______��
��______��
�ο��𰸣���֪A��F����ѧ��ѧ�г������ʣ�����A��C��E��FΪ���壬B��DΪҺ�壬D������������Ϊһ�����ҹ�ҵ����ˮƽ��һ�ֱ�־�ж�ΪH2SO4��AΪSO2��F��Ũ��Һ��X����ͨ������ʵ�����Ʊ�����C��X��һ�ֺ�ɫ��ĩ���жϷ�Ӧ���Ʊ������ķ�Ӧԭ����XΪMnO2��CΪCl2��FΪHCl��B��������18�����ӣ��Ͷ�������Ӧ�������ᣬ˵��B�����������ƶ�BΪH2O2����MnO2��Ӧ��������������ԭ������������EΪO2��
��1����ͼ����Ϣ������BΪH2O2��CΪSO2��XΪMnO2�������Դ�ǿ������˳�����ݷ�Ӧ��ϵ��H2O2+SO2=H2SO4��
H2O2+MnO2+H2SO4=MnSO4+2H2O+O2����MnO2+4HCl=MnCl2+Cl2��+2H2O��������������ԭ��Ӧ�������������Դ�����������õ���MnO2��Cl2��H2O2��
�ʴ�Ϊ��MnO2��Cl2��H2O2��
��2��BΪH2O2�ǹ��ۻ��������ʽΪ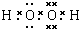
�����ڷ��Ӿ��壬�ʴ�Ϊ��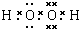
�����ӣ�
��3����Ӧ�ڵĻ�ѧ����ʽ��ͭ��Ũ���ᷴӦ��������ͭ�����������ˮ�ķ�Ӧ����Ӧ��ѧ����ʽΪ��Cu+2H2SO4��Ũ��?��?.?CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Cu+2H2SO4��Ũ��?��?.?CuSO4+SO2��+2H2O��
��4����Ӧ���������Ͷ���������ˮ��Һ�з����ķ�Ӧ������������ᣬ��Ӧ�����ӷ���ʽΪ��Cl2+SO2+2H2O�T4H++SO22-+2Cl-����Ӧ����ʵ�����Ʊ������ķ�Ӧ����Ӧ�����ӷ���ʽΪ��MnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��
�ʴ�Ϊ��Cl2+SO2+2H2O�T4H++SO22-+2Cl-��MnO2+4H++2Cl-?��?.?Mn2++Cl2��+2H2O��
���������
�����Ѷȣ�һ��
3������� ��8�֣���֪A�����Ǽ�ͥ�г�����һ�ֵ�ζ��������ɫ��Ӧ�ʻ�ɫ�� E����������ЧӦ����Ҫ����֮һ����Ӧ���ǹ�ҵ������������D�ķ�Ӧ����Ӧ����ʵ���Ҽ����� ����E�ķ�Ӧ���������з�Ӧ��ͼ��գ�
����E�ķ�Ӧ���������з�Ӧ��ͼ��գ�
��1��д���й����ʵ����ƻ�ѧʽ��
B?��C?��H?��
��2��д���ڷ�����Ӧ�Ļ�ѧ��Ӧ����ʽ
��������������������������������������������������������
д���ܷ�����Ӧ�Ļ�ѧ����ʽ������˫���ű�ʾ������ת�Ƶķ������Ŀ??������������������������������������������������������������������
�ο��𰸣���8�֣���1��д���й����ʵ����ƻ�ѧʽ��
B? H2O?��C? CaCO3?��L?Cl2?��(ÿ�գ���)
��2���ڻ�ѧ��Ӧ����ʽ? 2NaCl��2H2O 2NaOH��H2����Cl2��?��(2��)
2NaOH��H2����Cl2��?��(2��)
�ܻ�ѧ����ʽ?2Ca(OH)2��2Cl2==Ca(ClO)2��CaCl2��2H2O������˫�����ԣ�(���֣�
�����������
�����Ѷȣ�һ��
4������� A��B��C��D������ѧ��ѧ���������ʣ�����ɫ��Ӧ��Ϊ��ɫ���Ը�������ת����ϵ���ش��������⣺
��A
�ο��𰸣�A��B��C��D������ѧ��ѧ���������ʣ�����ɫ��Ӧ��Ϊ��ɫ��������Na��ɫ����Ӧ�ٷֽ�����B��ˮ��������̼����֪AΪNaHCO3��BΪNa2CO3����Ӧ��̼�������������Ʒ�Ӧ����̼�����C����CΪNaOH����Ӧ��D��ˮ��Ӧ����������NaOH����DΪNa2O2��A����NaOH��Ӧ����̼������ˮ��
��1��������������֪��AΪNaHCO3��BΪNa2CO3��DΪNa2O2��
�ʴ�Ϊ��NaHCO3��Na2CO3��Na2O2��
��2��ת���ٵĻ�ѧ����ʽΪ��2NaHCO3��.Na2CO3+CO2��+H2O��
ת���ܵ����ӷ���ʽΪ��OH-+HCO3-=CO32-+H2O��
�ʴ�Ϊ��2NaHCO3��.Na2CO3+CO2��+H2O��OH-+HCO3-=CO32-+H2O��
���������
�����Ѷȣ���
5��ѡ���� ��һ��������Һ�У�����NO3-��Iһ��Clһ��Fe3+�е�һ�ֻ������ӣ������Һ�м�����ˮ���嵥�ʱ���ԭ���ɴ��ƶ���Һ��? (? )
A��һ���е����ӣ�����ȷ���Ƿ���������
B��һ���������������
C��һ�����е����ӡ������ӡ����������
D�����������Ӻ����������
�ο��𰸣�AD
�����������
�����Ѷȣ���