时间:2020-07-07 23:57:47
1、选择题 某固体仅由一种元素组成,其密度为5g・cm-3。用X射线研究该固体得结果表明:在棱长1×10-7cm的立方体中含有20个原子,则此元素的相对原子质量最接近(?)
A.32
B.65
C.120
D.150
2、选择题 下列有关物理量相应的单位表达错误的是( )
A.摩尔质量g/mol
B.物质的量mol
C.溶解度g/100g
D.密度g/cm3
3、选择题 在一定温度和压强下,1体积的A2气体和3体积B2气体化合成2体积的C气体,则C的化学式为( )
A.AB3 B.AB C.A3B .A2B3
4、选择题 设NA为阿伏加德罗常数的值,下列叙述正确的是( )
A.18g重水(D2O)所含的电子数为10NA
B.22.4LCl2通入水中充分反应,共转移NA个电子
C.1L 1mol・L-1 NaF溶液中Fˉ的数目小于NA
D.25℃ 时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
5、选择题 相同物质的量浓度的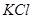 、
、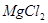 、
、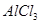 三种溶液,分别与体积相同、物质的量浓度相同的
三种溶液,分别与体积相同、物质的量浓度相同的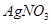 溶液恰好完全反应,消耗的这三种溶液的体积比是
溶液恰好完全反应,消耗的这三种溶液的体积比是
A.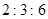
B.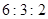
C.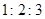
D.