ʱ��:2020-07-07 23:50:42
1��ѡ���� ����˵������ȷ����
A��8NH3(g)��6NO2(g)===7N2(g)��12H2O(g)����H<0����÷�Ӧһ�����Է�����
B����ȡ�����е�Ԫ��ʱ��Ϊ��I����ȫ����ΪI2����HNO3������������H2O2Ч����
C��ԭ��طŵ�����У���������һ�����ᣬ����������һ������
D������Ksp(MgCO3)<Ksp[Mg(OH)2]�����ˮ����MgCO3����ת��ΪMg(OH)2
�ο��𰸣�A
���������A��÷�Ӧ����������ӣ��������ӷ�Ӧ������S>0������G=��H���ԡ���S���ʸ÷�Ӧ��G���������Է����У�������H2O2Ч���ã����Ӿ��û��������ԭ��طŵ�����У�����������һ�����ᣬ��Ǧ���أ�����Ҫ���ӣ�����������Ҳ��һ�����ӣ���ͭпԭ��أ����������ӣ������ͬ�������ܵ���ʵ�Ksp���ܱȽ����ܽ�ȵĴ�С���ʸ����ȷ��
���������������ۺ��Ե���Ŀ��������������ԭ��Ӧ�Է����е�������������ȡ�⣬ԭ�������������ǰ��仯�����ܵ���ʵ��ܽ�ƽ��ȣ��ѶȽϴ�
�����Ѷȣ�һ��
2��ѡ���� ��֪��ˮ��Һ���������ɷ������з�Ӧ��I2+5Cl2+6H2O==2HIO3+10HCl��
���й��ڸ÷�Ӧ��˵������ȷ���ǣ�?��
A������������ԭ��Ӧ��
B����������ԭ��Ӧ��H2O�ǻ�ԭ��
C����������ԭ��Ӧ��I2ʧȥ����
D����������ԭ��Ӧ��Cl2ʧȥ����
�ο��𰸣�C
�����������
�����Ѷȣ���
3��ѡ���� ��֪����ԭ��ǿ����I����Fe2+����100 ml�⻯������Һ�л���ͨ��3��36 L(��״��)��������Ӧ��ɺ���Һ����1/2��Fe2+��������Fe3+����ԭ�⻯������Һ�����ʵ���Ũ��Ϊ
A��1��1mol��L��1
B��1��5mol��L��1
C��1��2mol��L��1
D��1��0mol��L��1
�ο��𰸣�C
����������⻯������Һ�д���I����Fe2+�����ڻ�ԭ��ǿ����I����Fe2+���ʻ���ͨ��3��36 L(��״��)������Cl2����I����Ӧ��2I��+ Cl2=I2+2Cl��������Fe2+��Ӧ��2Fe2++Cl2=2Fe3++2Cl������Ӧ��ɺ���Һ����1/2��Fe2+��������Fe3+���ʿ���ԭ�⻯������Һ�����ʵ���Ũ��Ϊxmol/L�����ݵ�ʧ�����غ��֪��0��1L��2xmol/L+0��1L��0��5xmol/L=0��3mol����x=1��2mol��L��1����C����ȷ��
���㣺������ԭ��Ӧ���㡣
�����Ѷȣ�һ��
4������� �����ܡ�����Ϊ21������߷�չDZ���������Դ��������ȼ��Ч�ʷdz��ߣ�ֻҪ�������м���4%���������Ϳ�ʹ��ȼ������40%��Ŀǰ�����ܼ������������ձ���ŷ�˵ȹ��Һ͵����ѽ���ϵͳʵʩ�Ρ���������ȡ�봢��������Դ����������о��ȵ㡣
��֪��CH4��g����H2O��g��=CO��g����3H2��g�� ��H��206.2 kJ��mol��1
CH4��g����CO2��g��=2CO��g����2H2��g�� ��H��247.4 kJ��mol��1
2H2S��g��=2H2��g����S2��g�� ��H��169.8 kJ��mol��1
��1���Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����
CH4��g����H2O��g����Ӧ����CO2��g����H2��g�����Ȼ�ѧ����ʽΪ________��
��2��H2S�ȷֽ�������ʱ������Ӧ����ͨ��һ������������ʹ����H2Sȼ�գ���Ŀ����____________��ȼ�����ɵ�SO2��H2S��һ����Ӧ���������ڳ����¾�Ϊ�����壬д���÷�Ӧ�Ļ�ѧ����ʽ��________________��
��3��H2O���ȷֽ�Ҳ�ɵõ�H2��������ˮ�ֽ���ϵ����Ҫ���������������¶ȵĹ�ϵ��ͼ1��ʾ��ͼ��A��B��ʾ������������________��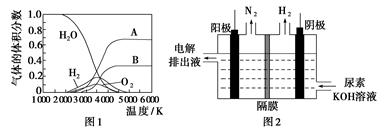
��4���������[CO��NH2��2]�ļ�����Һ�����װ��ʾ��ͼ��ͼ2�������и�Ĥ����ֹ����ͨ��������������Ϊ���Ե缫�������ʱ�������ĵ缫��ӦʽΪ________________��
��5��Mg2Cu��һ�ִ���Ͻ�350 ��ʱ��Mg2Cu��H2��Ӧ������MgCu2�ͽ���һ�ֽ���Ԫ�ص��⻯����������������Ϊ0.077����Mg2Cu��H2��Ӧ�Ļ�ѧ����ʽΪ____________��
�ο��𰸣���1��CH4��g����2H2O��g��=CO2��g����4H2��g�� ��H��165.0 kJ��mol��1
��2��ΪH2S�ȷֽⷴӦ�ṩ����
2H2S��SO2=2H2O��3S������4H2S��2SO2=4H2O��3S2����
��3��H��O������ԭ�ӡ���ԭ�ӣ�
��4��CO��NH2��2��8OH����6e��=CO32-��N2����6H2O
��5��2Mg2Cu��3H2 MgCu2��3MgH2
MgCu2��3MgH2
�����������1�����ݸ�˹���ɽ���һ���Ȼ�ѧ����ʽ���������ټ�ȥ�ڶ����Ȼ�ѧ����ʽ���ø��Ȼ�ѧ����ʽ����HҲ������Ӧ�ļ���æ�H��206.2 kJ��mol��1��2��247.4 kJ��mol��1��165.0 kJ��mol��1��
��2������ȼ�շ��ȣ�Ϊ��ֽ��ṩ����������Ͷ�������Ӧ���ɵ������ˮ��
��3��1 mol H2O�ֽ����ȵõ�2 mol H��1 mol O��������AΪH������BΪO��
��4������װ��ͼ��֪����������N2������������H2���ٷ���Ԫ�ػ��ϼ۵���������֪����H���õ�������������������[CO��NH2��2]ʧ��������N2��ͬʱ�ٽ�ϵ���غ�������غ��֪������CO32-��
��5������ԭ���غ�ͽ���Ԫ���⻯���������������Ϊ0.077���жϣ��ý���Ԫ�ص��⻯��ΪMgH2��
�����Ѷȣ�����
5��ѡ���� �����йػ�ѧ����ʽ��������ȷ���ǣ�������
A��������Һ��ͨ��������CO2��2C6H5O-+CO2+H2O��2C6H5OH+CO32-
B����֪C��ʯī��s��=C�����ʯ��s������H��0������ʯ��ʯī�ȶ�
C����20.0gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7kJ�����������ʾ�÷�Ӧ����ѧ������ʽΪ��NaOH��aq��+HCl��aq��=NaCl��aq��+H2O��1������H=-57.4kJ?mol-1
D����֪2C��s��+2O2��g��=2CO2��g������H12C��s��+O2��g��=2CO��g������H2�����H1����H2
�ο��𰸣�A��������̼���Ʒ�Ӧ��������Һ��ͨ��������CO2��Ӧ����̼�����ƣ�����ȷ�����ӷ�ӦΪC6H5O-+CO2+H2O�TC6H5OH+HCO3-����A����
B�����H��0����÷�ӦΪ���ȷ�Ӧ����ʯī�������ͣ�ʯī�ȶ�����B����
C��20.0gNaOH�����ʵ���Ϊ0.5mol���ų�28.7kJ����������1mol0gNaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�57.4kJ����������C��ȷ��
D������ȫȼ�շų����������ڲ���ȫȼ�շų�����������̼ȼ�յķ�Ӧ�ȡ�H��0�����H1����H2����D����
��ѡC��
���������
�����Ѷȣ�һ��