时间:2020-07-07 23:39:39
1、实验题 (16分)氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制流程: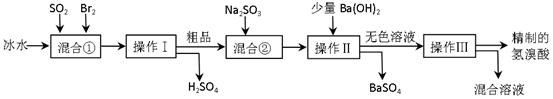
根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为?。
(2)混合①中使用冰水的目的是?。
(3)操作Ⅱ和操作Ⅲ的名称分别是?、?。
操作Ⅲ一般适用于分离____________混合物。(选填编号)
a.固体和液体? b.固体和固体? c.互不相溶的液体? d.互溶的液体
(4)混合②中加入Na2SO3的目的是?。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验加以探究:
甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为?,若假设成立可观察到的现象为?。
乙同学假设工业氢溴酸呈淡黄色是因为_______,其用于证明该假设所用的试剂为?。
2、填空题 工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2 7%,O2 11%,N2 82%):
| ?压强/MPa 转化率/% 温度/℃? | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
3、填空题 (16分)碳酸锂广泛应用于陶瓷和医药等领域。已 -锂辉石(主要成分为Li2O
-锂辉石(主要成分为Li2O Al2O3
Al2O3 4SiO2)为原材料制
4SiO2)为原材料制 备Li2CO3的工艺流程如下:
备Li2CO3的工艺流程如下: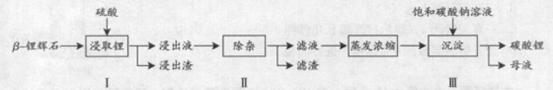
已知:Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4;Li2SO4、LiOH和Li2CO3在303K下的溶解度分别为34.2g、12.7g和1.3g。
(1)步骤Ⅰ前,B-锂辉石要粉碎成细颗粒的目的是_____________.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO42-,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入_____________(填“石灰石”、“氯化钙”或“稀硫酸”)以调节溶液的pH到6.0~6.5,沉淀部分杂质离子,然后分离得到浸出液。
(3)步骤II中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂技金属离子有
_________________。
(4)步骤III中,生成沉淀的离子方程式为________________。
(5)从母液中可回收的主要物质是__________________。
4、选择题 下列事实不能用勒沙特列原理解释的是
A.合成氨工业选择的反应条件不是室温,是500℃左右
B.配制氯化铁溶液时,将氯化铁加入盐酸中,然后加水稀释
C.实验室常用排饱和食盐水的方法收集氯气
D.硫酸工业中,使用过量的空气以提高二氧化硫的利用率
5、选择题 绿色化学对于化学反应提出了“原子经济性”的新概念及要求。理想的原子经济性反应是原料中的原子全部转变成所需产物,不生成副产物,实现零排放。在下列氮肥的制备反应中,原子利用率最高的是
[? ]
A.NH3+H2O+CO2=NH4HCO3
B.
C.8NH3+3Cl2=N2+6NH4Cl
D.NH3+NaCl+CO2+H2O = NH4Cl+NaHCO3