时间:2020-07-07 23:33:01
1、选择题 设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是? (? )
A.1mol NH3所含有的原子数为NA
B.常温常压下,22.4L氧气所含的原子数为2NA
C.常温常压下,48g O3所含的氧原子数为3NA
D.1 L 0.1mol/LNaCl溶液中所含的Na+为NA
参考答案:C
本题解析:A错1mol NH3所含有的原子数为3NA;B错,应为标准状况下;C正确;D错,1 L 0.1mol/LNaCl溶液中所含的Na+为0.1NA
本题难度:简单
2、填空题 硫酸试剂瓶标签上的部分内容如图。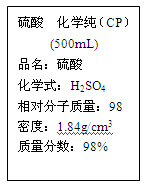
据此回答下列问题:
(1)该硫酸的物质的量浓度为 mol/L。
(2)配制250mL 0.50mol・L-1的稀硫酸需取该硫酸 mL。
(3)配制时必需的玻璃仪器有: 。
(4)定容时,若加入的水超过刻度线,必须采取的措施是 。
(5)下列操作会使所配溶液浓度偏低的是 。
A.转移溶液时,未洗涤烧杯
B.容量瓶用蒸馏水洗净后仍残留蒸馏水
C.定容时,俯视容量瓶的的刻度线
D.定容摇匀后,发现液面低于刻度线,再加水至刻度线
参考答案:(1)18.4 (2)6.8
(3)量筒、250mL容量瓶、烧杯、玻璃棒(容量瓶未写规格扣1分)
(4)重新配制溶液 (5)AD
本题解析:(1)硫酸质量为500乘以1.84乘以0.98等于901.6克,则硫酸物质的量为901.6除以98等于9.2mol,则硫酸物质的量浓度为9.2除以0.5等于18.4 mol/L;(2)稀释前后溶质物质的量不变,即250乘以0.5等于18.4V,则V等于6.8mL;(3)配制一定物质的量浓度溶液所需的仪器:量筒、250mL容量瓶、烧杯、玻璃棒;(4)定容时,若加入的水超过刻度线,必须采取的措施是重新配制溶液;(5)A、溶质的量减少,所配的浓度偏低;B、定容时还需加蒸馏水,所以容量瓶用蒸馏水洗净后仍残留蒸馏水,对实验结果无影响;C、定容时,俯视容量瓶,所配的溶液浓度偏高;D、定容后,再加水,相等于稀释溶液,浓度偏低。
考点:考查配制一定物质的量浓度溶液的相关知识点。
本题难度:困难
3、选择题 4g NaOH溶于水配成50mL溶液,溶液的物质的量浓度是
A.2mol/L
B.0.2 mol/L
C.1 mol/L
D.0.1 mol/L
参考答案:A
本题解析:因为n=m/M,所以4g氢氧化钠是0.1mol。又因为c=n/V,所以溶液的浓度是0.1mol÷0.05L=2mol/L,答案选A。
本题难度:一般
4、选择题 等质量的下列物质中,所含分子数最少的是
[? ]
参考答案:D
本题解析:
本题难度:简单
5、选择题 下列溶液中的C1-的物质的量浓度与150.0mL l.0 mol/L CaCl2溶液中的Cl-物质的量浓度相等的是
A.150 .0mL 1 .0 mol/L NaCl溶液
B.75 .0mL 2.0 mol/L MgCl2溶液
C.150 .0mL 2 .0 mol/LKCl溶液
D.75.0 mL 1 .0 mol/L A1C13溶液
参考答案:C
本题解析:A选项,150.0mL1.0mo1/L NaCl溶液中氯离子的浓度为1mol/L,与题意不符,故A错误;B选项,75.0mL2.0mol?L-1MgCl2溶液中氯离子的浓度为2mol/L×2=4mol/L,与题意不符,故B错误;C选项,150.0mL2.0mo1.L-1KCl溶液中氯离子的浓度为2mol/L,与题意相符,故C正确;D选项,75.0mL1.0mol?L-1A1C13溶液中氯离子的浓度为1mol/L×3=3mol/L,与题意不符,故D错误。
本题难度:一般