ʱ��:2020-07-07 23:25:57
1��ѡ���� 2013���ŵ������ѧ���ٴ�������㻯ѧ����Ŀ�ѧ�ҡ����»��ڽṹ���۽��з��Ѽ���ó�����
A����Ȼ������ֵ
B���ϳɰ���ԭ��������
C�����صĺ�����
D��p��������Ƶ���״
�ο��𰸣�D
���������2013��10��9�գ�2013��ŵ������ѧ��������������̫���������ۻ�ѧ��������������˹(Martin Karplus)������˹̹����ѧ��������ѧ�����˶�����ά��(Michael Levitt)���ϼ��ݴ�ѧ��ѧ������Ү����л��(Arieh Warshel)������ӻ�ѧ��ϵ����˶�߶�ģ�Ͷ�������������ṩ�𰸣�D��ȷ��
�����Ѷȣ���
2��ѡ���� �����մɵĺϳɷ����ǽ��մɣ���Ҫ�ɷ֣�Al2O3��ZrO2�����²��ϣ���ճ���������Ҫ��Cr��Mo��W��Ti�ȸ��۵��������ĥ���ȳ��ͺ����ս�ʹ������Ȼ�Ե��ʵ���ʽ�����ڽ����մ�֮�У��ݴ��жϺϳɹ��ձ���
[? ]
A. �������кϳ�
B. ��HCl�����кϳ�
C. �ڵ��������кϳ�
D. �ڿ����кϳ�
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� ��6�֣���ҵ�ϳɰ����Ʊ�����һ��������������������£�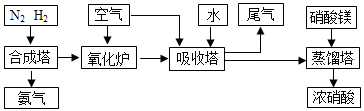
��1���ںϳɰ��ķ�Ӧ�У��ı䷴Ӧ��������ʹƽ�ⷢ���ƶ�������ͼ���ʾ�������ı䣬�����İٷֺ����ı仯���ơ�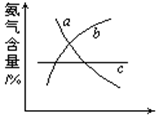
��������Ϊѹǿʱ���仯������ȷ���ǣ�ѡ����ĸ��ţ�_________��
��������Ϊ�¶�ʱ���仯������ȷ���ǣ�ѡ����ĸ��ţ�?��
��2����ͼ��ʾ�����ݻ���ͬ�������١��ڡ��ۣ�����ʼ�¶���ͬ��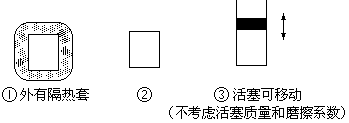
�ֱ������������г���3mol H2��1mol N2��һ�������·�Ӧ���ﵽƽ��ʱ��������NH3���ʵİٷֺ�����С�����˳��Ϊ?����������ţ�
�ο��𰸣���6�֣� (1) b��?a ?��2���٣��ڣ���
�����������Ӧ�ص㣺N2��g����3H2��g���P2NH3��g��?��H��0��
��1��ѹǿ����ƽ�������ƶ������İٷֺ����������£�ƽ�������ȷ����ƶ������������ƶ������İٷֺ�����С��
��2���ۺ��¡���ѹ������3mol H2��1mol N2 ����Ӧ������У�����������С������������ں��¡����ݣ��൱���ڢ۵Ļ����Ͻ��м�ѹ������ƽ�⽫�������ƶ����İٷֺ������Ӧ�ڢ����½��ģ����ڣ��ۣ��ٺ��ݣ����и����ף���Ӧ���У���Ӧ���ȣ��൱���ڢڵĻ����Ͻ��м��Ȳ�����ƽ�⽫�������ƶ�,���İٷֺ����½������٣��ڡ�
�����Ѷȣ�һ��
4��ѡ���� ����˵������ȷ����