1、选择题 许多小溪流经硫矿和金属矿,由于含硫矿暴露在空气中或暴露在含氧的水中,这些小溪变成酸性,溪水中含有溶解的铁和硫酸盐,它们的浓度都很高。最常见的含硫矿是黄铁矿(FeS2),其中铁的化合价为+2;当富铁的溪水和其他水混合时,溶于水的铁以针铁矿[FeO(OH)]的形式沉淀出来,覆盖在小溪的底部,而水仍保持酸性。反应的离子方程式为4Fe2++O2+6H2O=4FeO(OH)↓+xH+,则该离子方程式中H+的化学计量数x为(? )
A.5
B.6
C.7
D.8
2、填空题 (9分)“温室效应”是全球关注的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决温室效应的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有:?。(填字母)
a.减少化石燃料的使用? b.植树造林,增大植被面积
c.采用节能技术? d.利用太阳能、风能
(2)将CO2转化成有机物可有效实现碳循环。CO2转化成有机物的例子很多,如:
 以上反应中,最节能的是?,原子利用率最高的是?。
以上反应中,最节能的是?,原子利用率最高的是?。
(3)文献报道某课题组利用CO2催化氢化制甲烷的研究过程如下:

反应结束后,气体中检测到CH4和H2,滤液中检测到HCOOH,固体中检测到镍粉和Fe3O4。CH4、HCOOH、H2的产量和镍粉用量的关系如下图所示(仅改变镍粉用量,其他条件不变):

研究人员根据实验结果得出结论:
HCOOH是CO2转化为CH4的中间体,即: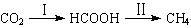
①写出产生H2的反应方程式?。
②由图可知,镍粉是?。(填字母)
a.反应Ⅰ的催化剂? b.反应Ⅱ的催化剂? c.反应Ⅰ、Ⅱ的催化剂? d.不是催化剂
③当镍粉用量从1 mmol增加到10 mmol,反应速率的变化情况是?。(填字母)
a.反应Ⅰ的速率增加,反应Ⅱ的速率不变
b.反应Ⅰ的速率不变,反应Ⅱ的速率增加
c.反应Ⅰ、Ⅱ的速率均不变
d.反应Ⅰ、Ⅱ的速率均增加,且反应Ⅰ的速率增加得快
e.反应Ⅰ、Ⅱ的速率均增加,且反应Ⅱ的速率增加得快
f.反应Ⅰ的速率减小,反应Ⅱ的速率增加
3、选择题 2006年1月1日,我省“苏北五市”决定全面推广使用乙醇汽油作为发动机燃料,即在汽油中掺入一定比例的乙醇,以代替一部分汽油。下列有关说法正确的是
A.乙醇汽油是一种清洁能源,燃烧不会产生污染
B.乙醇与汽油组成元素相同,化学成分相似
C.乙醇汽油燃烧时,耗氧量高于等质量的汽油
D.乙醇可通过淀粉转化制得,是一种可再生的燃料
4、选择题 化学与科学、技术、社会及生自学成才密切相关。下列做法或说法不正确的是
[? ]
A.研发高效低毒的农药,降低作物的农药残留量
B.用可降解的无毒聚乳酸塑料代替聚乙烯作食品包装袋,以防止白色污染
C.驾驶家用汽车代替公交车参观世博园,以便节能减排
D.对干旱地区,适时在云层播散化学物质,实施人工降雨,以缓解旱情
5、选择题 下面是人们对于化学科学的各种常见认识,其中错误的是( ? )
A.化学是一门以实验为基础的自然科学
B.化学是一门具有较强实用性的科学
C.化学支持高新技术的快速发展,但面对伪科学和人体健康等问题却显得无能为力
D.化学将为解决能源问题、环境问题、资源问题等提供有效途径和方法
微信搜索关注"91考试网"公众号,领30元,获取公务员事业编教师考试资料40G