时间:2020-07-07 23:23:52
1、填空题 (14分)(1)物质的量浓度均为0.1 mol/L的下列溶液:①NH4Cl、②Na2CO3、③NaHCO3、④NaHSO4、⑤CH3COOH、⑥NaOH,pH由大到小的顺为: (填数字代号)
(2)氢气燃烧热值高。实验测得,在常温常压下,1 g H2完全燃烧生成液态水,放出142.9 kJ热量。则H2燃烧的热化学方程式为 _____________________ _____________。
(3)常温下,0.1 mol/L的NaHCO3溶液的pH大于8,则溶液中C(H2CO3)___ _C( CO32-) (填>、=或<),原因_________ ____
(用离子方程式和必要的文字说明)
(4)常温下,pH=a某强酸溶液V1 L,pH=b某强碱溶液V2 L,已知a+b=12,两溶液混合后pH=7,求V1 和V2的关系
(5)25℃下,某Na2SO4溶液中c(SO42-)=5×10-4 mol·L-1,取该溶液1 mL,加水稀释至10 mL,则稀释后溶液中c (Na+)∶c (OH-)=____ ____
(6)常温下,已知Ksp(Mg(OH)2)=1.8×10-11,则Mg(OH)2在pH=12.00的NaOH溶液中的Mg2+浓度
为 mol·L-1
参考答案:(1)⑥②③①⑤④;(2)2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ?mol-1;
(3)>;因为NaHCO3溶液中既存在电离平衡:HCO3-?CO32-+H+,又存在水解平衡:HCO3-+H2O?H2CO3+OH-,而HCO3-水解程度大于电离程度.;(4)V2=102V1;(5)1000:1;(6)1.8×10-7
本题解析:NaHSO4为强酸的酸式盐,c(H+)=0.1mol/L;NaOH为强碱,c(OH—)=0.1mol/L;CH3COOH为弱酸,NaOH的PH最大、NaHSO4的PH最小;NH4Cl水解溶液呈酸性;Na2CO3、NaHCO3水解呈碱性,Na2CO3的水解程度大于NaHCO3,所以PH由大到小的顺为⑥②③①⑤④;(2)2 mol H2完全燃烧生成液态水,放出4×142.9 kJ热量,H2燃烧的热化学方程式为2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ?mol-1;(3)HCO3—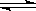 H++ CO32—电离呈酸性、HCO3—+H2O
H++ CO32—电离呈酸性、HCO3—+H2O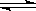 H2CO3+OH-,水解呈碱性,溶液的pH大于8,说明水解大于电离,C(H2CO3)>C( CO32-);(4)
H2CO3+OH-,水解呈碱性,溶液的pH大于8,说明水解大于电离,C(H2CO3)>C( CO32-);(4)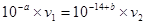 ,
,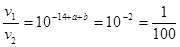 ;(5)c(SO42-)=5×10-4 mol·L-1,c (Na+)=1×10-3 mol·L-1,Na2SO4溶液呈中性,所以c (OH-)= 1×10-7 mol·L-1;c (Na+)∶c (OH-)= 1000:1;(6)pH=12.00的NaOH溶液中c (OH-)= 1×10-2 mol·L-1,
;(5)c(SO42-)=5×10-4 mol·L-1,c (Na+)=1×10-3 mol·L-1,Na2SO4溶液呈中性,所以c (OH-)= 1×10-7 mol·L-1;c (Na+)∶c (OH-)= 1000:1;(6)pH=12.00的NaOH溶液中c (OH-)= 1×10-2 mol·L-1,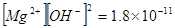 ,所以Mg2+浓度为1.8×10-7mol·L-1。
,所以Mg2+浓度为1.8×10-7mol·L-1。
考点:本题考查水溶液。
本题难度:困难
2、选择题 常温下,下列对有关溶液的判断不正确的是(?)
A.Na2CO3溶液中,c(OH-) = c(H+)+c(HCO3–)+c(H2CO3)
B.温度相同、浓度相同的①(NH4)2SO4、②NaNO3、③NH4HSO4、④NH4NO3、⑤ 、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是:③①④②⑥⑤
、⑥CH3COONa溶液,它们的pH值由小到大的排列顺序是:③①④②⑥⑤
C.NaA溶液的pH=8,c(Na+)-c(A-) = 0.99×10-6 mol/L
D.10 mL pH = 12的氢氧化钠溶液中加入pH = 2的HA至pH刚好等于7,所得溶液体积V(总)≤20mL
参考答案:A
本题解析:根据质子守恒c(OH-) = c(H+)+c(HCO3–)+2c(H2CO3)可知,选项A不正确。其余都是正确的,答案选A。
本题难度:简单
3、选择题 在0.1 mol/L的NaAc(醋酸钠)溶液中,欲使c(Na+)/c(Ac-)比值减小,可采取的措施是(?)
A.加热
B.加少量水
C.加少量盐酸
D.加少量醋酸钠晶体
参考答案:D
本题解析:略
本题难度:简单
4、选择题 室温时,将xmLpH=a的稀NaOH溶液与ymL pH=b的稀盐酸充分反应。下列关于反应后溶液pH的判断,正确的是( )
A.若x=y,且a+b=14,则pH>7
B.若10x=y,且a+b=13,则pH=7
C.若ax=by,且a+b=13,则pH=7
D.若x=10y,且a+b=14,则pH>7
参考答案:D
本题解析:由题可知,n(NaOH)=x×10-3×10a-14mol,n(HCl)= y×10-3×10-bmol。
故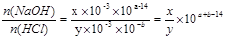 ,分步讨论:
,分步讨论:
(1)若x=y,,则n(NaOH)=n(HCl),二者恰好反应,pH=7
(2)若10x=y,且a+b=13,则n(HCl)=100n(NaOH),HCl过量,pH<7
(3)若ax=by,且a+b=13,则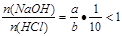 (因a>7,b<7),HCl过量,
(因a>7,b<7),HCl过量,
(4)若x=10y,且a+b=14,则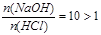 ,NaOH过量,pH>7
,NaOH过量,pH>7
所以答案选D。
点评:混合溶液pH的计算要注意过量问题。
本题难度:一般
5、填空题 液氨与水性质颇为相似,其电离方程式可表示为:2NH3 NH4++NH2-。某温度下其离子积常数为1×10-30(mol·L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
NH4++NH2-。某温度下其离子积常数为1×10-30(mol·L-1)2。液氨中的pNH4与水中的pH类似,向1L液氨中加入2.3gNa此时上述平衡____________移动(填“向正方向”“向逆方向”或“不”),完全反应后溶液的pNH4=__________。
参考答案:(1)向正方向
(2)29
本题解析:2.3gNa加入液氨后发生反应2Na+2NH4+=2Na++2NH3+H2↑, c(NH4+)减小,平衡向正反应方向移动,2.3gNa的物质的量为0.1mol,所以生成NH2-的物质的量为0.1mol,c(NH4+)=1×10-30(mol·L-1)/ 0.1mol·L-1= 1×10-29mol·L-1,pNH4+=29
本题难度:简单