ʱ��:2019-07-04 01:56:53
1��ѡ���� ������Һ�и�����Ũ�ȹ�ϵ����ȷ����
A��0.1mol��L��1 HCOOH��Һ�У�c(HCOO-)��c(OH��)��c(H��)
B��0.1mol��L��1 NH4Cl��Һ�У�c(NH4+)+c(NH3?H2O)��c(Cl-)
C��0.1mol��L-1NaHCO3��Һ�У�c(Na+)+c(H+)+c(H2CO3)��c(HCO3-)+c(CO32-)+c(OH-)
D��������������ʵ���Ũ�ȵ�CH3COONa������CH3COOH��Ϻ����Һ�У�c(CH3COO-)
�ο��𰸣�
���������
�����Ѷȣ�һ��
2��ѡ���� pH=1������һԪ��HX��HY��Һ���ֱ�ȡ100mL����������þ�ۣ���ַ�Ӧ���ռ���H2����ֱ�ΪVHX��VHY������ͬ������VHX>VHY��������˵����ȷ�� ��?��?
A��HX������ǿ��
B��HYһ����ǿ��
C��HX������ǿ��HY������
D����Ӧ��ʼʱ��������H2���������
�ο��𰸣�B
���������pH=1������һԪ��HX��HY��Һ���ֱ�ȡ100mL����������þ�ۣ���ַ�Ӧ���ռ���H2����ֱ�ΪVHX��VHY������ͬ������VHX>VHY��˵��HXһ�������ᣬ��ѡB��
��������Ũ�ȵ�������ᣬ��������п��Ӧ�����ɵ�����һ���ࣻ��PH������һԪ��HX��HY��Һ����������п��Ӧ������������������ᣬ��Ϊ��������ӻ�������һ���������ӣ����Ҳ��ת����Ϊ������
�����Ѷȣ�һ��
3������� ����֪����ᡢ���ᡢ�����ᣨHCN����̼���������µĵ��볣���ֱ�Ϊ��
| �� | HF | Ka=6.8��10-4mol?L-1 �� CH3COOH Ka=1.7��10-5mol?L-1 �� HCN Ka=6.2��10-10mol?L-1 �� H2CO3 Ka1=4.4��10-7mol?L-1 Ka2=4.7��10-11mol?L-1 |
�ο��𰸣���1����������HF�ĵ���ƽ�ⳣ�������HF����ǿ��HCN�ĵ���ƽ�ⳣ����С����HCN����������
�ʴ�Ϊ��HF��HCN��
��2��̼��Ϊ��Ԫ���ᣬ�ֲ����룬�Ե�һ������Ϊ�������뷽��ʽΪH2CO3?HCO3-+H+��HCO3-?CO32-+H+��
�ʴ�Ϊ��H2CO3?HCO3-+H+��HCO3-?CO32-+H+��
��3������ǿ��HF��H2CO3��HCN��HCO3-���ɷ�����Ӧ����NaF��CO2����Ӧ�ķ���ʽΪ2HF+Na2CO3�T2NaF+H2O+CO2����������CO2ͨ��NaCN��Һ�У������ķ�Ӧ����ʽΪNaCN+H2O+CO2�THCN+NaHCO3��
�ʴ�Ϊ��2HF+Na2CO3�T2NaF+H2O+CO2����NaCN+H2O+CO2�THCN+NaHCO3��
��1����ˮϡ�ʹٽ�һˮ�ϰ����룬����Ũ��ˮ��һˮ�ϰ�Ũ������ƽ�������ƶ�������Ũ���ᣬ�����������ӷ�Ӧ�ٽ�һˮ�ϰ����룬���Դٽ�һˮ�ϰ��������ABD��
���������������ƣ�c��OH-����������һˮ�ϰ����룬���������Ȼ�泥�c��NH4+����������һˮ�ϰ����룬��������һˮ�ϰ��������CE��
�ʴ�Ϊ��ABD��CE��
��2������Һ�м���Ũ��ˮ���ٽ�һˮ�ϰ����룬��Һ��c��NH4+����c��OH-��������
����Һ�м���ˮ���ٽ�һˮ�ϰ����룬��笠����ӻ���������������ı���С����Һ�������ı���������c��NH4+����c��OH-������С��
�ʴ�Ϊ��A��B��
��3������Һ�м����Ȼ�泥�笠�����Ũ����������һˮ�ϰ����룬������������Ũ�ȼ�С������Һ�м����������ƹ��壬��Һ������������Ũ����������һˮ�ϰ����룬��笠�����Ũ�ȼ�С��
�ʴ�Ϊ��E��C��
���������
�����Ѷȣ���
4��ѡ���� ���Թ���ij��ɫ��Һ���ȣ���Һ��ɫ��dz����ԭ��Һ������
�ٵ���ʯ���NH4Cl��Һ?�ڵ��з�̪�İ�ˮ��Һ?�۵���ʯ���H2SO4��Һ?�ܵ��з�̪�ı�������������Һ?�ݵ��з�̪��Na2CO3��Һ?������SO2��Ʒ����Һ
A���ڢ�
B���٢ۢ�
C���٢ܢ�
D���ڢ�
�ο��𰸣�A
����������� NH4Cl��ǿ�������Σ�����Һ��NH4+ˮ������Һ�����ԣ����Եμ�ʯ����Һ��Һ��Ϊ��ɫ��������ˮ�ⷴӦ�����ȷ�Ӧ�����������¶ȣ�NH4Clˮ��̶�������Һ��������ǿ����Һ��ɫ������ڰ�ˮ�Լ��ԣ��μӷ�̪��Һ��Ϊ��ɫ�����Թܼ��ȣ����ڰ�ˮ���ȶ����������ֽ⣬�����ݳ�����Һ�ļ��Լ��������Ժ�ɫ��dz����ȷ����H2SO4��Һ�����Եģ���ʹ��ɫʯ����Һ��Ϊ��ɫ����������ǿ����ʣ��ȶ���ǿ������ʱ�Ȳ��ֽ⣬Ҳ���ٵ��룬������Һ�ĺ�ɫ���䡣��������������ǿ���ʹ��ɫ�ķ�̪��Ϊ��ɫ�������ܽ�����¶ȵ����߶����ͣ����Ը��Թ��е�ʱ��������������Һ����ʱ�����ܽ�ȵļ�Сc��OH-�����ͣ���Һ�ļ��Լ��������Ժ�ɫ��dz����ȷ����Na2CO3��ǿ��������ˮ��ʹ��Һ�Լ������Եμӷ�̪��Һ��Ϊ��ɫ�����������¶ȴٽ��ε�ˮ�⣬���Լ����Թ�ʱ��ɫ�������Ʒ����Һ�Ǻ�ɫ�ģ�����������SO2��ʱ������SO2��Ư���ԣ�������Һ����ɫ������ɫ���ʲ��ȶ����������ֽ⡣���Ը��Թ��е����ʼ���ʱ��Һ�ֱ�Ϊ��ɫ������
�����Ѷȣ�һ��
5������� ��֪HA��һ�����ᡣ��ش��������⣺
��1������һ�ֺ���HA��������NaA����Һ��
����ɸ���Һ����������?��
���������Һ�м�����������ʱ��������Ӧ�����ӷ���ʽ��?��
���������Һ����μ���NaOH��Һʱ������ͼ���ܱ�ʾ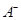 ������Ŀ�仯���Ƶ���?(����ĸ)��
������Ŀ�仯���Ƶ���?(����ĸ)��
��2���ֽ�1���0.04mol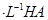 ��Һ��1���0.02mol
��Һ��1���0.02mol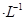 NaOH��Һ��ϣ��õ�2��������Һ��
NaOH��Һ��ϣ��õ�2��������Һ��
�����û��Һ�Լ��ԣ�����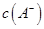 ?0��01 mol
?0��01 mol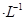 (�<������=����>��)��
(�<������=����>��)��
�����û��Һ�����ԣ�����Һ���������ӵ�Ũ���ɴ�С��˳����?��
�ο��𰸣���1����H2O��HA��H+��Na+��OH?��A-��2�֣��д����÷֣�
��A-+H+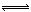 HA��2�֣���д�����Ҳ�ɣ�
HA��2�֣���д�����Ҳ�ɣ�
��D��1�֣�
��2����<��1�֣�
��c(A-)>c(Na+)>c(H+)>c(OH?)��2�֣�
�����������1������Һ�е������ӼȰ������ӣ�Ҳ�������ӣ����Ժ���HA��������NaA����Һ���������У�H2O��HA��H+��Na+��OH?��A-
�ڼ����������ᣬHCl��NaA��Ӧ����HA���������ӷ���ʽΪ��A-+H+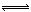 HA
HA
����Һ����HA��NaA����μ���NaOH��Һ��HA��NaOH��Ӧ����NaA��H2O������A2-��Ŀ������D����ȷ��
��2����1���0.04mol/LHA��Һ��1���0.02mol/LNaOH��Һ��ϣ�HA�������õ�������NaA��HA�����û��Һ�Լ��ԣ���c(H+)<c(OH?)�����ݵ���غ�c(H+)+c(Na+)=c(OH?)+c(A-)�ɵ�c(A-)<0.01mol?L?1��
�����û��Һ�����ԣ���HA�ĵ���̶ȴ���NaA��ˮ��̶ȣ���Һ���������ӵ�Ũ���ɴ�С��˳���ǣ�c(A-)>c(Na+)>c(H+)>c(OH?)
�����Ѷȣ�һ��