时间:2019-07-04 01:00:04
1、填空题 (6分)常见金属单质A、B和非金属单质C、D以及它们化合物之间的转化关系如下。F、J既能溶于强酸M又能溶于强碱N,Z的摩尔质量为198 g・mol-1,且其中各元素的质量比为:
钾 : 金属B? : 氧=39 : 28 : 32。
请回答下列问题:
(1)Z的化学式为: ▲ 。
(2)写出检验X中阳离子的方法: ▲ 。
(3)写出E和A在高温下反应的化学方程式为: ▲ 。
(4)写出A和N反应的离子方程式: ▲ 。
参考答案:(1)K2FeO4(1分)
(2)取试样少许,滴加3~4滴KSCN溶液,呈血红色(1分)
(3)8 Al+3Fe3O4 ?4Al2O3+9Fe(2分)
?4Al2O3+9Fe(2分)
(4)2Al+2OH―+2H2O=2AlLO2-+3H2↑(2分)
本题解析:略
本题难度:简单
2、填空题
图所示的关系。
试回答下列问题:
(1)G的化学式为:?。
(2)写出下列反应的化学方程式
①?,
②?。
(3)X在医药上用作解酸剂,与盐酸作用时,生成B的物质
的量与消耗盐酸的物质的量之比为3:8,则X的化学
式为:?。
参考答案:(7分)(1)NaOH(1分)(2)①2Na2O2+2CO2=2Na2CO3+O2(2) (2分)③3MgCO3・Mg(OH)2或Mg4(OH)2(CO3)3等;(2分)
(2分)③3MgCO3・Mg(OH)2或Mg4(OH)2(CO3)3等;(2分)
本题解析:此题是无机推断题,考查了元素化合物的知识。题眼是H是常见金属单质, I是常见非金属单质,又根据关系图,可知H+B=A+I,此为点燃条件下置换反应,且为金属置换非金属,初步确定为2Mg+CO2=2MgO+C,所以A为MgO,A由X分解得到,且X为碱式盐,应为碱式碳酸镁,B是CO2,C可能为H2O,二者均能和D反应,且都生成F,F是常见非金属单质,可知D为过氧化钠,F为氧气。其余可推知。(3)中根据X和盐酸反应,生成CO2的物质的量与消耗盐酸的物质的量之比为3:8,当生成CO2是3时,消耗盐酸为6,其余盐酸相当于和OH-反应,为2。推得结果为3MgCO3・Mg(OH)2或Mg4(OH)2(CO3)3。
本题难度:一般
3、填空题 (8分)A、B、C、D四种物质之间有下图所示的转化关系。已知:A是一种非金属单质,为黄色晶体;B、C、D均为化合物;B是形成酸雨的主要成分之一。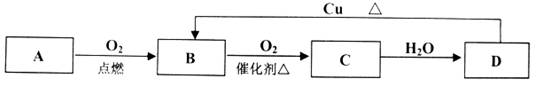
请回答下列问题:
(1)化合物B是_______(填化学式,下同),化合物D是___________;
(2)B→C化学反应的类型是________反应(填“化合”、“分解”、“置换”或“复分解”)
(3)向D的稀溶液中滴加BaCl2溶液,能产生白色沉淀。写出该反应的离子方程式:
__________________________________________________。
参考答案:(1)SO2?H2SO4?(2)化合? (3)Ba2++SO42-=BaSO4↓
本题解析:(1)B是形成酸雨的主要成分之一,可知B为SO2,则非金属单质A为S,C为SO3,D为H2SO4。
(2) SO2与O2反应生成SO3是两种物质生成一种化合物,属于化合反应。
(3)向硫酸稀溶液中滴加BaCl2溶液,生成硫酸钡沉淀和盐酸,离子方程式为Ba2++SO42-=BaSO4↓
故答案为:(1)SO2?H2SO4?(2)化合? (3)Ba2++SO42-=BaSO4↓
本题难度:一般
4、填空题 (A、B、C为短周期元素.A为常见的金属,B在常温下为固体,它的最高价氧化物的水化物D为常见强酸,C的最高价氧化物的水化物E为常见强碱.A、B、C及化合物的其转化关系如图: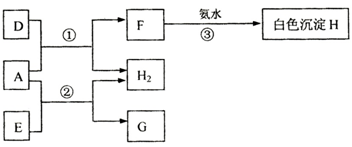
请回答下列问题:
(1)写出D的化学式______,B与C形成的化合物的电子式为______;
(2)写出反应③的离子方程式______.
(3)标准状况下,等质量的A分别与足量的D、E反应,产生H2的体积分别为V1、V2,其关系为V1______V2(填<、>或=).若V2=2.24l,则反应过程中转移的电子的物质的量为______.
参考答案:A、B、C为短周期元素,A为常见的金属,B在常温下为固体,它的最高价氧化物的水化物D为常见强酸判断为H2SO4,C的最高价氧化物的水化物E为常见强碱和金属A反应生成氢气,推断E为NaOH,A既可以和强酸反应也可以和强碱反应判断为Al,A和D(H2SO4)反应生成的F为硫酸铝,H为Al(OH)3,G为NaAlO2,结合上述推断得到B为硫元素,C为钠元素;
(1)D的化学式为:H2SO4;B与C形成的化合物为Na2S的电子式为: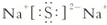
故答案为:H2SO4 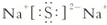
;
(2)反应③是硫酸铝和氨水反应生成氢氧化铝沉淀的过程,反应的离子方程式为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
(3)标准状况下,等质量的A(Al)分别与足量的D(H2SO4)、E(NaOH)反应,产生H2的体积分别为V1、V2,依据电子守恒得到生成氢气体积相同;若V2=2.24l,n(H2)=0.1mol则反应过程中转移的电子的物质的量为0.2mol;
故答案为:0.2mol;
本题解析:
本题难度:一般
5、简答题 a、b、c、d、e是含有一种相同元素的五种物质,可发生如图转化:其中:a是单质;b是气体;c、d是氧化物;e是最高价氧化物对应的水化物.
(1)如果a是一种淡黄色粉末固体,试推断这五种物质(用名称表示):
a______;b______;c______;d______;e______.
并写出由c生成d的化学方程式______
(2)如果a为单质且是一种常见气体,试推断这五种物质(用化学式表示):
a______;b______;c______;d______;e______.
并写出由d生成e的化学方程式______.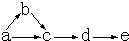
参考答案:淡黄色单质为硫,题中能发生连续氧化,对应的反应有硫和氮元素的转化:
(1)a物质是淡黄色粉末,且能够被连续两次氧化,所以a物质是非金属硫,b为硫化氢,c为二氧化硫,d为三氧化硫,e为硫酸,c生成d的反应为2SO2+O2催化剂
本题解析:
本题难度:一般