时间:2019-07-04 00:59:43
1、填空题 (Ⅰ)将铜丝的一端绕成螺旋状,在酒精灯外焰加热,冷却后变黑。再在酒精灯上将该铜丝加热至红热状态。 如右图所示,趁热插入到试管里的氯化铵晶体中,在试管中出现白烟。冷却后取出铜丝,可看到铜丝变成光亮的紫红色。回答下列问题: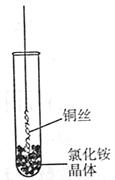
⑴解释“当红热的铜丝插入氯化铵晶体中,出现白烟”的原因(用化学方程式表示)?。
⑵灼热的氧化铜在氯化铵中变成单质铜,写出该反应的化学方程式?
?。
( II)2008年,我国的航天事业取得了巨大的成就,航天员翟志刚顺利实现了太空行走。在航天发射时,肼(N2H4)及其衍生物常用作火箭推进剂。
⑴N2H4・H2O能发生类似NH3・H2O的微弱电离,使溶液显示弱碱性,该电离分两步,写出第一步电离的方程式?。
⑵在实验室中,用N2H4・H2O与NaOH颗粒一起蒸馏,收集114~116℃的馏分即为无水肼。
①在蒸馏过程中不需要的仪器是?(填序号字母)。
A.酒精灯
B.长直玻璃导管
C.锥形瓶
D.冷凝管
E.牛角管(接液管)? F.蒸馏烧瓶? G.酸式滴定管
②除上述必需的仪器外,还缺少的玻璃仪器是?。
⑶肼能使锅炉内壁的铁锈(主要成分Fe2O3)变成磁性氧化铁(Fe3O4)层,可减缓锅炉锈蚀。若反应过程中肼转化为氮气,每生成1molFe3O4,需要消耗肼的质量为??g。
2、实验题 (16分)铜与浓硫酸反应,实验装置如图所示。
(1) 装置A中发生反应的化学方程式为:?,反应过程中试管B中的现象是?,试管C的作用是?。
(2) 导管D的下端(虚线段)应位于?(液面上、液面下),导管D的作用有:①实验结束后排除装置中的SO2;②?。
实验中发现试管内除了产生白色固体外,在铜丝表面还有黑色固体甲生成,甲中可能含有CuO、Cu2O、CuS、Cu2S。为探究甲的成分,进行了以下的实验。
查阅资料可知:Cu2O + 2HCl =CuCl2+ Cu + H2O, 2Cu2O + O2煅烧 4CuO,2CuS+3O2煅烧2CuO+2SO2,Cu2S+2O2煅烧2CuO+SO2。CuS、 Cu2S和稀HCl不反应。
 (3) 固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有:?。
(3) 固体乙在空气中煅烧时,使用的实验仪器除了玻璃棒、三脚架、酒精灯外,还必须有:?。3、选择题 下列关于铁及其化合物的说法中正确的是
A.Fe3O4是―种红棕色粉末,俗称磁性氧化铁
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.去除FeCl2溶液中的FeCl3杂质可以向溶液中加入过量铁粉,然后过滤
D.Fe3+与KSCN反应产生红色沉淀
4、选择题 把铜粉和铁粉的混合物,放入一定量的稀硝酸中,微热,反应完毕发现铜有剩余,则溶液中含有的阳离子是?
A.Cu2+、Fe2+
B.Cu2+、Fe2+、Fe3+
C.Cu2+、Fe3+
D.Fe3+
5、实验题 Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为?;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式:?。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol・L-1 H2SO4、0.01 mol・L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
| 实验步骤 | 预期现象与结论 |
| 步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 | ? ?; |
| 步骤2:____________________________________ ____________________________________。 | ? |