时间:2019-07-03 23:57:53
1、填空题 (12分)已知A是生产生活中用量最大的金属,B为淡黄色粉末。在常温下C为无色液体,E、G、H、I、J为气体,其中H为黄绿色,其它为无色。J能使湿润的红色石蕊试纸变蓝(图中部分产物已略去)。 ?
?
请填写下列空白
(1)写出化学式:D?,K?。
(2)写出②的离子方程式?。
(3)反应④不属于下列何种反应类型?(填字母序号)。
A. 化合反应? B. 氧化还原反应? C. 离子反应? D. 置换反应
(4)若要确定③反应后所得溶液中含有M物质,所选试剂为?(填序号)。
A. KSCN溶液和氯水? B. 铁粉和KSCN
C. 浓氨水? D. 酸性高锰酸钾溶液
(5)将F加入到M的溶液里并露置在空气中,可以观察到整个过程的现象是:
?。
(6)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式?。
参考答案:(1)Fe3O4,NH4Cl(2分,各1分)
(2)2Na2O2+2H2O =4Na++4OH―+O2↑(2分)
(3)D(1分)(4)D(3分)
(5)产生白色沉淀,迅速变成灰绿色,最后变成红褐色(2分)
(6)8NH3+3Cl2=N2+6NH4Cl(2分)
本题解析:由题中所给信息,A是金属铁,常温下C为无色液体只能是水,A能和水蒸气反应生成D(四氧化三铁)和E(氢气)。H为黄绿色,所以H是氯气,I是氯化氢。又有J能使湿润的红色石蕊试纸变蓝也是解本题的突破口,可得J为氨气,所以K为NH4Cl。B为淡黄色粉末,可能是单质硫、过氧化钠、溴化银等,依据转化关系可知B只能是过氧化钠,其和水反应生成G(氧气)和F(氢氧化钠),F(氢氧化钠)和K(NH4Cl)反应生成无色气体J(氨气)。
D(四氧化三铁)和I(氯化氢)的溶液反应生成N(氯化铁)和M(氯化亚铁),M(氯化亚铁)可以和H(氯气)反应生成N(氯化铁)。检验③反应后所得混合溶液中M(氯化亚铁)的存在,不能选A、B、D,因为溶液中存在显黄色的三价铁离子,所以只能用氨水检验。
点评:本题主要考查根据题给信息和实验现象正确判断物质类别,解答推断题要抓住几个重要的突破口,如物质的颜色、反应溶液的颜色等。
本题难度:困难
2、填空题 有A、B、C、D、E五种透明溶液,它们分别是盐酸、AgNO3、BaCl2、NaCl、Na2CO3,按下面顺序两两混合,其现象如下表:
若A为Na2CO3,则B~E分别是:?B?;C?;D?;E?。
参考答案:
本题解析:略
本题难度:一般
3、推断题 某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。
请回答下列问题。
(1)图中涉及分离溶液与沉淀的方法是__________________。
(2)B、C、D、E 4种物质的化学式为:B_________、C_________、D_________、E_________。
(3)沉淀F与NaOH溶液反应的离子方程式为__________________________________。
沉淀E与稀硫酸反应的离子方程式为__________________________________________。
溶液G与过量稀氨水反应的化学方程式为______________________________________。
参考答案:(1)过滤?(2)Al2O3?Fe2O3?NaAlO2?Al(OH)3?
(3)Al2O3+2OH-=2AlO2―+H2O
Al(OH)3+3H+=Al3++3H2O
Al2(SO4)3+6NH3・H2O=2Al(OH)3↓+3(NH4)2SO4
解析:本题主要考查铝的化合物的性质。Al、Al2O3、Al(OH)3的反应多发生在酸性或碱性环境中;溶液的酸碱性决定了铝元素的成盐形式为Al3+或AlO2―。
本题解析:A溶于水得沉淀和溶液,硫酸铝易溶于水,氧化铝、氧化铁不易溶于水,所以得到的溶液是硫酸铝溶液(即G),沉淀F是氧化铝和氧化铁,将沉淀F溶于过量氢氧化钠溶液中,氧化铝能和氢氧化钠反应,氧化铁和氢氧化钠不反应,所以沉淀C是氧化铁,溶液D是偏铝酸钠。硫酸铝和氨水反应生成氢氧化铝和硫酸铵,所以溶液沉淀E是氢氧化铝,将沉淀氢氧化铝加热得到B,B是氧化铝。
(1)分离溶液和固体的操作是过滤。
(2)由以上分析得,B、C、D、E4种物质分别为Al2O3、Fe2O3、NaAlO2、Al(OH)3。
(3) 沉淀F是氧化铝和氧化铁,将沉淀F溶于过量氢氧化钠溶液中,氧化铝能和氢氧化钠反应,氧化铁和氢氧化钠不反应,反应的离子方程式为Al2O3+2OH-=2AlO2―+H2O。沉淀E是氢氧化铝,与稀硫酸反应的离子方程式为Al(OH)3+3H+=Al3++3H2O。溶液G是硫酸铝溶液,与过量稀氨水反应的化学方程式为Al2(SO4)3+6NH3・H2O=2Al(OH)3↓+3(NH4)2SO4。
点评:本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质,然后顺推或逆推或由两边向中间推得出其他物质。
本题难度:一般
4、推断题 有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物已略)。其中,B、D、E、F均为无色气体,M、L为常见的金属单质,C为难溶于水的红褐色固体。在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和M反应可放出大量的热。请回答下列问题: 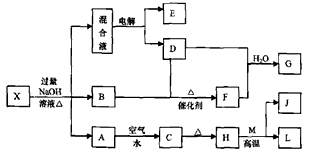
(1)B的电子式为______________。
(2)画出元素M的原子结构示意图_______________。
(3)物质X的化学式为____________________________。
(4)电解混合液时阳极反应式为_______________________________。
(5)按要求写出上述转化关系中有关反应的化学方程式:①含有L元素的化合反应____________________________。②含有L元素的置换反应___________________________。
(6)已知E气体在D中完全燃烧生成稳定的化合物时,放出kJ的热量,写出E燃烧热的热化学方程式___________________________________。
参考答案:(1)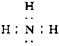 ?
?
(2)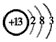
(3)(NH4)2Fe(SO4)2
(4)4OH--4e-=O2↑+2H2O
(5)4Fe(OH)2+O2+2H2O=4Fe(OH)3;Fe2O3+2Al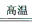 2Fe+Al2O3
2Fe+Al2O3
(6)H2(g)+O2(g)=H2O(1);△H= kJ/mol
kJ/mol
本题解析:
本题难度:一般
5、填空题 (4分)根据下图所示,推断物质X的化学式。X的化学式?
参考答案:NaNO3
本题解析:根据转化关系可知,X中应该含有钠离子。在常见的强酸中还有硝酸,所以X应该是硝酸钠。即氢氧化钠和硝酸反应,碳酸钠和硝酸反应,硫酸钠和硝酸钡,氯化钠和硝酸银即能满足。
本题难度:一般