时间:2019-07-03 23:57:53
1、填空题 (15分)物质A、E、F的焰色反应呈黄色,物质I的1个分子由4个原子组成并共含有10个电子,B、C、D、K在常温下都是气体单质,G在常温下是无色液体,反应①~⑤都是用于工业生产的反应,各有关物质之间的相互反应转化关系如下图所示(部分反应条件已略去):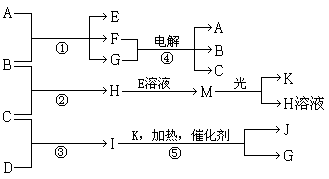
(1)写出物质的化学式:B?M?
(2)写出A物质的电子式?物质I是?分子(填极性或非极性)
(3)0.1mol/LE水溶液中各离子浓度由大到小的顺序为?
(4)反应①的离子方程式?
反应⑤的化学方程式?
(5)反应④中,若转移0.02mol电子后停止反应,溶液的体积是200mL,则此时溶液(不考虑电解产物的相互反应)的PH=_________。
参考答案:(1)B:Cl2? M:HClO 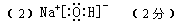 ?极性? (注意:此空1分,其余每空2分)
?极性? (注意:此空1分,其余每空2分)
(3)c(Na+)>c(ClO-)>c(OH-)>c(H+)
(4)Cl2+2OH-=Cl-+ClO-+H2O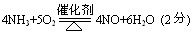
(5)13
本题解析:物质I的1个分子由4个原子组成并共含有10个电子,所以I是氨气,则C是氢气,D是氮气。G在常温下是无色液体,因此G是水,则K是氧气,J是NO。A、E、F的焰色反应呈黄色,所以A是氢氧化钠,B是氯气,E是次氯酸钠,F是氯化钠,H是氯化氢,M是次氯酸。
(1)略
(2)氢氧化钠是含有离子键和极性键的离子化合物,电子式为 。氨气是三角锥形,所以是极性分子。
。氨气是三角锥形,所以是极性分子。
(3)次氯酸钠是强碱弱酸盐,水解显碱性,所以离子浓度大小顺序是c(Na+)>c(ClO-)>c(OH-)>c(H+)。
(4)见答案
(5)惰性电极电解食盐水的方程式为2NaCl+2H2O 2NaOH+Cl2↑+H2↑,转移0.02mol电子时生成氢氧化钠是0.02mol,其浓度是0.1mol/L,所以pH=13。
2NaOH+Cl2↑+H2↑,转移0.02mol电子时生成氢氧化钠是0.02mol,其浓度是0.1mol/L,所以pH=13。
本题难度:一般
2、填空题 (12分)根据下列框图关系填空。已知常温下X为无色液体,D、E均为无色气体,
G是一种主要的工 业产品。C的焰色反应为黄色,E、F的相对分子量之间的关系为
业产品。C的焰色反应为黄色,E、F的相对分子量之间的关系为
M(F)=M(E)+16。回答下列问题: 
(1)A中化学键的类型为?,写出B的一个用途?。
(2)将固体A加入CuSO4溶液中的主要现象是? ??。
??。
(3)写出气体B的水溶液与CuSO4溶液反应的离子方程式??。
(4)写出反应②的化学方程式,若是氧化还原反应,请标出电子转移的方向和数目。
?
(5)经测定,反应④中每生成1.0gX,放出3.2KJ的热量(常温下)。试写出反应④的热化学方程式?。
参考答案:(共12分)(1) 非极性共价键 离子键 (各1分) ;制硝酸或制冷剂等(1分)
(2)无色 气体、蓝色沉淀(2分)(其他合理答案也给分)
气体、蓝色沉淀(2分)(其他合理答案也给分)
(3)2NH3.H2O+Cu2+=Cu(OH)2↓+2NH4+ (2分)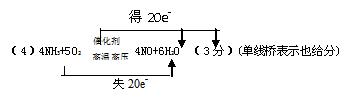
(5)NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(l) ;△H=" ―57.6kJ/" mol?(2分)
本题解析:略
本题难度:一般
3、简答题 已知:甲、乙、丙为常见单质,甲常温下为固体,乙为一黄绿色气体,丙为无色气体.A、B、C、D均为化合物,D为一红褐色沉淀,它们之间有下图转化关系.请回答以下问题.
(1)写出下列物质的化学式;乙______;B______.
(2)写出③反应的化学方程式:______.
(3)写出②反应的离子方程式:______.
参考答案:本题的解题关键是乙为一黄绿色气体直接判断为氯气;D为一红褐色沉淀判断为氢氧化铁;结合甲、乙、丙为常见单质,甲常温下为固体,丙为无色气体.A、B、C、D均为化合物,通过转化关系图逐一分析判断个物质的组成和反应;由D是氢氧化铁可知,A+NaOH→Fe(OH)3,推断A是含铁的氯化物,确定A为FeCl3,甲为Fe;转化图中 A+甲→B,是发生了Fe+2Fe3+=3Fe2+,B+NaOH→C,发生的是Fe2++2OH-=Fe(OH)2↓;C+丙→D,发生的反应是:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
综上所述:转化关系中的各物质分别为,
甲:Fe;乙:Cl2;丙:O2;A:FeCl3;B:FeCl2;C:Fe(OH)2;D:Fe(OH)3;
依据上述分析和判断回答下列问题:
(1)乙的化学式为Cl2;B的化学式FeCl2;
故答案为:Cl2?FeCl2?
(2)第③反应的化学方程式是被氧气氧化为氢氧化铁的反应,氧化亚铁化学方程式为4Fe(OH)2+2H2O+O2=4Fe(OH)3
故答案为:4Fe(OH)2+2H2O+O2=4Fe(OH)3
(3)第②反应的离子方程式是氯化铁和铁发生的氧化还原反应,溶液中反应的离子方程式为:Fe+2Fe3+=3Fe2+;
故答案为:Fe+2Fe3+=3Fe2+
本题解析:
本题难度:一般
4、推断题 (14分)淡黄色固体X和气体A存在如下转化关系:
请回答下列问题:
(1)固体X的名称 ?;A的化学式 ??。
(2)写出反应①③的化学方程式,并指出氧化剂。
反应① ?, ?。
反应③ ?, ?。
(3)写出②④反应的离子方程式:
反应② ?。
反应④ ?。
参考答案:(除特殊标注外,每空2分,共14分)(1) 过氧化钠? CO2
(2)2Na2O2 + 2CO2=2Na2CO3 + O2? Na2O2?(1分)
2Na + O2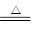 ?Na2O2? O2?(1分)
?Na2O2? O2?(1分)
(3)Ca2++CO32-= CaCO3↓? CaCO3 + 2H+=Ca2+ + H2O + CO2↑
本题解析:淡黄色固体X和气体A可以反应生成气体和该题,这说明X应该是过氧化钠,则气体B是氧气。固体Y能和石灰水反应生成白色沉淀,所以Y是碳酸钠,则A是CO2,白色沉淀是碳酸钙。
点评:该题是高考中的常见题型,试题综合性强,难度较大,对学生的要求较高。该题学生需要明确化学推断题是一类综合性较强的试题,如元素及化合物性质和社会生活,环境保护,化学计算等知识,还可引入学科间综合。它不仅可考察学生对化学知识的理解程度,更重要的是培养学生的综合分析能力和思维方法。解框图题的方法:最关键的是寻找“突破口”,“突破口”就是抓“特”字,例如特殊颜色、特殊状态、特殊气味、特殊反应、特殊现象、特殊制法、特殊用途等。
本题难度:困难
5、推断题 下图各物质中,A、B、C是常见金属单质,甲、乙、丙是气体且乙是有特殊颜色的气体(图中有些反应的产物和反应的条件没有全部标出)。 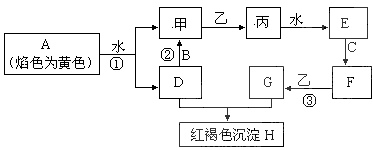
请根据以上信息回答下列问题:
(1)写出:H的化学式_________,乙的两种重要用途________________________________
(2)写出有关反应的离子方程式:反应①______________________ 反应②_______________________
(3)判断反应③己经发生的常用试剂是______________________
(4)胶态磁流体(液溶胶)在医学上有重要用途, C单质对应元素的某种纳米级氧化物是磁流体中的重要粒子,该磁流体的主要制备过程如下:(Ⅰ)将NH3通入F、G的混合溶液(F、G物质的量比为1:2)中会生成两种碱。(Ⅱ)这两种碱恰好反应就得到 该氧化物。写出(Ⅱ)中反应的化学方程式为:_________________________,确定该磁流体己成功制取的方法_________________________________
参考答案:(1)Fe(OH)3;制造盐酸、漂白剂、农药、合成纤维、消毒杀菌等
(2)2Na+2H2O===2Na++2OH-+H2↑;2Al+2OH-+2H2O===2AlO2-+3H2↑
(3) KSCN(其它合理的答案也对)
(4)Fe(OH)2 + 2Fe(OH)3===Fe3O4 + 4H2O;做丁达尔实验,能产生丁达尔现象(其它合理答案也对)。
本题解析:
本题难度:一般