ʱ��:2019-07-03 23:57:53
1������� ��10�֣���ĩ״��ƷA���ɵ����ʵ�����MgO��Al2O3�볣������������B��ɵĻ���A������ͼ��ʾ��ת����ϵ�� ?
?
������������⣺?
(1)����C��H�Ļ�ѧʽ�ֱ���__________��__________��
(2)д����I����J�����ӷ���ʽ��_____________________________________
(3)д����F����G�����ӷ���ʽ________________________________________
(4)��10.7 g��ƷA��MgO��Al2O3��B�����ʵ�����Ϊ0.05? mol����B�Ļ�ѧʽΪ_________��
�ο��𰸣���10�֣���ÿ��2�֣�(1)Al��Cl2?(2)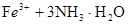 ===
===
(3) ===
=== ? (4)FeO
? (4)FeO
������������ɫ����J����JӦ��������������������I�������ữ����������Ӧ���ɰ�ɫ����������K���Ȼ�������I���Ȼ�����D�ǵ�������H����������˵��A�н���������BӦ�������������ͨ�����ȷ�Ӧ���ɵ�����������C��Al��E������þ������������������ɵĻ�������þ������������Һ����Ӧ������F��ƫ�����ƺ��������ƵĻ���ƫ�����ƺ�CO2��Ӧ��������������ɫ��������G���������������������ֽ⼴������������0.05mol����þ���������������ֱ���2g��5.1g������B��������10.7g-2g-5.1g=3.6g�����B����Է���������3.6��0.05=72����B��FeO��
��������ѧ�ƶ�����һ���ۺ��Խ�ǿ�����⣬��Ԫ�ؼ����������ʺ�������������������ѧ�����֪ʶ����������ѧ�Ƽ��ۺϡ��������ɿ���ѧ���Ի�ѧ֪ʶ������̶ȣ�����Ҫ��������ѧ�����ۺϷ���������˼ά���������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȡ�
�����Ѷȣ�һ��
2��ѡ���� ��ͼװ�ó���ͨ������X�����ڹܿ�P����ȼ��ʵ����ʹ����ʯ��ˮ����ǣ���X��Y�����ǣ���������H2��NaHCO3 ��CO��Na2CO3 ��CO��CuO?��H2��Fe2O3��
A���٢�
B���٢�
C���ڢ�
D���ۢ�
�ο��𰸣�B
���������
�����Ѷȣ���
3������� A��B��C��D��E����ѧ������5�ֻ����A��B�������Ԫ��X��Y�ĵ����������г����Ľ�����������ʼ�Ĺ�ϵ��ͼ��ʾ��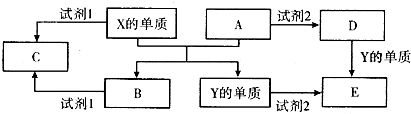
��ش��������⣺
��1��X�ĵ�����A��Ӧ�Ļ�ѧ����ʽ��______��
��2�����Լ�1��NaOH��Һ��X�ĵ������Լ�1��Ӧ�����ӷ���ʽ��______��
��3�����Լ�1���Լ�2����ϡ���ᣮ
�ټ�������D����Һ�н������ӵķ�����______��
�ڽ�����C����ˮ������Һ�����ԣ�ԭ���ǣ������ӷ���ʽ��ʾ��______��
��ij��Ч��ˮ������Y��OH��S04�ۺϵõ��ģ���ҵ����E��ϡ�������������Ϊԭ�����Ʊ�Y��OH��SO4����Ӧ����NO���ɣ��÷�Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣�Ԫ��X��Y�ĵ����������г����Ľ�����Y�����������XΪAl��YΪFe��A��B���������Al����������Ӧ����Fe����������Al�����������������ᷴӦ������Ӧ����Fe���������������ᷴӦ�����Լ�1ΪNaOH��Һʱ��CΪƫ�����ƣ��Լ�2Ϊ����ʱ��DΪ��������EΪ�����������Լ�1Ϊ����ʱ��CΪ������������Һˮ�������ԣ�
��1��X�ĵ�����A��ӦΪ���ȷ�Ӧ����Al����������Ӧ������������Fe���÷�ӦΪFe2O3+2Al?����?.?Al2O3+2Fe��
�ʴ�Ϊ��Fe2O3+2Al?����?.?Al2O3+2Fe��
��2�����Լ�1��NaOH��Һ����Al��NaOH��Һ��Ӧ����ƫ�����ƺ����������ӷ�ӦΪ2Al+2H2O+2OH-�T2AlO2-+3H2�����ʴ�Ϊ��2Al+2H2O+2OH-�T2AlO2-+3H2����
��3�����Լ�1���Լ�2����ϡ���ᣬ
��DΪ�����������������ӵķ���Ϊȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ���ɫ����֤��ԭ��Һ�к���Fe3+��
�ʴ�Ϊ��ȡ������Һ���Թ��У��μӼ���KSCN��Һ����Һ���ɫ����֤��ԭ��Һ�к���Fe3+��
��CΪ��������ˮ�������ԣ�ˮ�����ӷ�ӦΪAl3++3H2O 
Al��OH��3+3H+��
�ʴ�Ϊ��Al3++3H2O 
Al��OH��3+3H+��
��EΪ������������ϡ�������������Ϊԭ������Fe��OH��SO4����Ӧ����NO���ɣ��÷�ӦΪ2FeSO4+2NaNO2+H2SO4�T2Fe��OH��SO4+Na2SO4+2NO����
�ʴ�Ϊ��2FeSO4+2NaNO2+H2SO4�T2Fe��OH��SO4+Na2SO4+2NO����
���������
�����Ѷȣ�һ��
4������� ��8�֣���ͼ����ѧ��ѧ�г�������֮����ת����ϵ������C������Ư�ף�������M�������ӻᵼ������ЧӦ����Ӧ�۳�����ʵ������ȡ����B��
��ش��������⣺
�� ?C�ķ���ʽΪ?��J�ĵ���ʽΪ?��
�� д����Ӧ�ٵ����ӷ���ʽ?��
�� д����Ӧ�ڵĻ�ѧ����ʽ?��
��?C��M�����ƵĻ�ѧ���ʣ���Ҳ��������C��Ư���ԡ�M��Ư���ԡ�?C��M����������ͬ��ѧ���ʵ�ԭ����?��
�ο��𰸣�
���
������������������Ŀ�ͼ����ʽ������Ԫ�ػ�������Ƶ��������ͻ�ƿ��У�H�ǻ���ɫ���壬ӦΪCl2��J��ɫ��ӦΪ��ɫ����KԪ�أ���G����Һ��⣬���������ⱥ��ʳ��ˮ���Ӷ�ȷ����GΪKCl����Ӧ��Ϊʵ������ȡ����ķ�Ӧ��������Ϊ����MnO2�ļ��ȷ�Ӧ�����ѵó�KΪKClO3��BΪO2��GΪKCl����Ԫ���غ�֪����Ӧ�ڵIJ���EΪˮ��AΪ����ɫ��δ��C����Ư�ף���BΪO2�����ƶϳ�AΪS��CΪSO2��DΪSO3��FΪH2SO4��M�������ӻᵼ������ЧӦ����ΪCO2���壬��LΪ̼��
�����Ѷȣ�һ��
5������� ����ͼ��ʾ�Ļ�ѧ��Ӧ��ͼ���⣮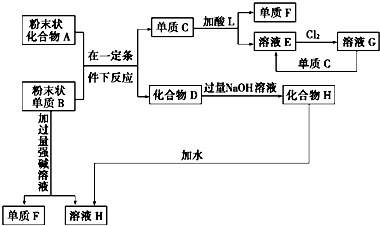
��1������ F��______����ҺH����������Ҫ������______��
��2��д�����з�Ӧ�Ļ�ѧ����ʽ��
C+L-��F+E��______��
B-��F+H��______��
��3��д�����з�Ӧ�����ӷ���ʽ��
E+Cl2-��G��______��
G+C-��E��______��
D-��H��______��
��4����C-��E+F������Ũ�ᣬ����ѡ�õ�Ũ����______���ѧʽ����
�ο��𰸣�����ͼʾ��Ϣ������֪��A+B��C+D�ķ�Ӧ�����û���Ӧ������B���Ժ�ǿ�����������Ʒ�����Ӧ��˵��BΪ����������AΪ��������CΪ��������DΪ�����������������Ժ��ᷴӦ���������κ������������ο��Ժ�������Ӧ�����������Σ�����ת�����������֪��E���Ȼ�������F��������LΪ���ᣬGΪ�Ȼ��������������Ժ��������Ʒ�Ӧ����HΪƫ�����ƣ����������Ժ��������Ʒ�Ӧ����ƫ�����ƺ�������
��1������F��������ƫ���������ڿ�����ˮ���Σ���Һ�е�������Ҫ�ǣ�Na+��AlO2-��OH-���ʴ�Ϊ��H2��Na+��AlO2-��OH-��
��2��������������ķ�ӦΪ��Fe+2HCl�TFeCl2+H2�������������Ժ��������Ʒ�Ӧ����ƫ�����ƺ���������2Al+2NaOH+2H2O�T2NaAlO2+3H2����
�ʴ�Ϊ��Fe+2HCl�TFeCl2+H2����2Al+2NaOH+2H2O�T2NaAlO2+3H2����
��3���������Խ�������������Ϊ���������ӣ���2Fe2++Cl2�T2Fe3++2Cl-�����������Ժ����������ӻ��������������ӣ���2Fe3++Fe�T3Fe2+������������������������Ժ�ǿ�Ӧ����ƫ�����ƺ�ˮ����Al2O3+2OH-�T2AlO2-+H2O��
�ʴ�Ϊ��2Fe2++Cl2�T2Fe3++2Cl-��2Fe3++Fe�T3Fe2+��Al2O3+2OH-�T2AlO2-+H2O��
��4�����������Ժͷ������Ե��ᷴӦ���������κ����������Ǻ������Ե��ᷴӦ���ɵ����������Σ�������������������Ե������������Ũ����ȣ��ʴ�Ϊ��HNO3��H2SO4��
���������
�����Ѷȣ�һ��