时间:2019-07-03 23:52:20
1、选择题 下列叙述正确的是(?)
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol?L-1的盐酸,与等体积水混合后pH=1
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
参考答案:C
本题解析:加热促进水的电离,但纯水仍然显中性,A不正确。醋酸是弱酸,稀释有利于电离,所以稀释至10倍后pH<4,B不正确。盐酸是强酸,所以0.2 mol?L-1的盐酸,与等体积水混合后浓度是0.1mol/L,所以pH是1,C正确。pH=3的醋酸溶液的浓度大于10-3mol/L,所以和氢氧化钠反应后,醋酸是过量的,因此溶液显酸性,D不正确。所以答案选C。
本题难度:一般
2、选择题 下列条件中可以促进水的电离的是
A.升高温度
B.加入少量固体氢氧化钾
C.加入少量固体氯化钠
D.滴加少量浓盐酸
参考答案:A
本题解析:A.升高温度,水的电离程度增大
B加入少量固体氢氧化钾,氢氧根离子浓度增大,抑制水的电离
C加入少量固体氯化钠,对水的电离无影响
D滴加少量浓盐酸,抑制水的电离。
所以促进水电离的只有A。
本题难度:一般
3、选择题 下列叙述正确的是?(?)
A.向CH3COONa的稀溶液中加入少量CH3COONa晶体,则溶液中的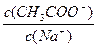 比值变大
比值变大
B.体积为VL的Na2CO3溶液pH=a,加水后使其体积为10V时,其溶液的pH=a-1
C.pH=11的KOH溶液与pH=3的醋酸溶液等体积混合,滴入酚酞后溶液呈红色
D.硫酸铵溶液中加入适量氨水,当溶液的pH=7时,c(SO2-4)>c(NH+4)
参考答案:A
本题解析:醋酸钠溶液中加入少量醋酸钠晶体,溶液浓度会增大,醋酸根离子浓度与钠离子浓度的比值等于醋酸根离子物质的量与钠离子物质的量之比,应分子分母均变化不一比较。变换思维,向醋酸钠溶液中加入少量水,溶液浓度会变稀,醋酸根离子的水解程度增大,分母钠离子的物质的量不变,分子醋酸根离子的物质的量减小,分式的值减小。相反增大浓度分式的值增大。
本题难度:一般
4、选择题 在一定条件下,氢气和丙烷燃烧的化学方程式为:
2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ?mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l)△H=-2220kJ?mol-1
1mol?氢气和2mol丙烷的混合气完全燃烧时放热为( )kJ.
A.4500
B.2791.6
C.1681.6
D.4725.8
参考答案:氢气和丙烷燃烧热分别为:285.8kJ/mol,2220kJ/mol,
所以1mol?氢气和2mol丙烷的混合气完全燃烧时放热为285.8kJ/mol×1mol+2220kJ/mol×2=4725.8kJ,
故选D.
本题解析:
本题难度:简单
5、选择题 100 mL pH=2的两种一元酸x和y,稀释过程中pH与溶液体积的关系如图所示。下列说法正确的是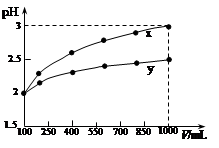
A.稀释前x、y的物质的量浓度相等
B.x为强酸,y为弱酸
C.随着稀释的进行,y的电离程度减小
D.等体积的x、y分别分别与足量的锌反应,x放出的氢气多
参考答案:B
本题解析:根据图像可知,稀释10倍,X的pH从2变为3,所以X是强酸,但Y的pH从2变为2.5,这说明在稀释过程中,有氢离子电离出来,所以Y是弱电解质,因此B正确。A不正确,稀释前Y的浓度大,C不正确,稀释促进电离。D不正确,应该是是Y发出的氢气多,答案选B。
本题难度:简单