时间:2019-07-03 23:52:20
1、选择题 下列微粒中不能破坏水的电离平衡的是:
A.Na HSO4
B.Al3+
C.CO32-
D.K+
参考答案:D
本题解析:
NaHSO4电离出H+,抑制水的电离平衡;Al3+、CO32-水解,促进水的电离平衡
本题难度:一般
2、选择题 有关常温下pH均为3的醋酸和硫酸的说法正确的是? ( )
A.两种溶液中,由水电离出的氢离子浓度均为1×10-11 mol/L
B.分别加水稀释100倍后,两种溶液的pH仍相同
C.醋酸中的c(CH3COO-)和硫酸中的c(SO)相等
D.分别加入足量锌片,两种溶液生成H2的体积相同
参考答案:A
本题解析:略
本题难度:简单
3、选择题 下列说法正确的是
A.在101kPa时,1mol物质完全燃烧时所放出的热量,叫做该物质的燃烧热
B.酸和碱发生中和反应生成1mol水,这时的反应热叫中和热
C.燃烧热或中和热是反应热的种类之一
D.在稀溶液中,1molCH3COOH和1mol NaOH完全中和时放出的热量为57.3kJ
参考答案:C
本题解析:本题旨在考查对燃烧热、中和热的定义的理解,特别是两概念中应注意的问题
本题难度:简单
4、选择题 已知温度T时水的离子积常数为 。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
。该温度下,将浓度为amol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的pH=7
C.混合溶液中,
D.混合溶液中,
参考答案:C
本题解析:A.因酸碱的强弱未知,a=b,只能说明酸碱恰好完全反应,但如为强酸弱碱盐或强碱弱酸盐,则溶液不呈中性,故A错误;B.因温度未知,则pH=7不一定为中性,故B错误;C.混合溶液中, ,根据c(H+)?c(OH-)=KW,可知溶液中c(OH-)=
,根据c(H+)?c(OH-)=KW,可知溶液中c(OH-)= ,溶液呈中性,故C正确;D.任何溶液都存在电荷守恒,即c(H+)+c(B-)=c(OH-)+c(A-),不能确定溶液的酸碱性,故D错误;故选C。
,溶液呈中性,故C正确;D.任何溶液都存在电荷守恒,即c(H+)+c(B-)=c(OH-)+c(A-),不能确定溶液的酸碱性,故D错误;故选C。
本题难度:一般
5、填空题 (8分)已知下列热化学方程式:①2H2(g) +O2(g)=2H2O(l);ΔH= -570 kJ・mol-1
②2H2(g) +O2(g)=2H2O(g) ΔH= -483.68 kJ・mol-1
③2C(s) +O2(g)=2CO(g) ΔH=-221 kJ・mol-1
④ C(s) +O2(g)=CO2(g) ΔH= -393.5 kJ・mol-1
回答下列问题:
(1)H2的燃烧热为 ;C的燃烧热为 。
(2)燃烧10gH2生成液态水,放出的热量为 。
(3)写出CO燃烧的热化学方程式 。
参考答案:(1)285KJ/mol、393.5KJ/mol (2)1425KJ
(3)CO(g) +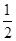 O2(g)=CO2(g);ΔH=-283KJ/mol
O2(g)=CO2(g);ΔH=-283KJ/mol
本题解析:(1)燃烧热是在一定条件下,1mol可燃物完全燃烧生成稳定的氧化物时所放出的热量。所以氢气的燃烧热是285KJ/mol。C的燃烧热为393.5KJ/mol。
(2)10g氢气是5mol,放出的热量是285KJ/mol×5mol=1425KJ。
(3)④×2-③得到2CO(g) +O2(g)=2CO2(g) ΔH= -566 kJ・mol-1 。
本题难度:一般