时间:2019-07-03 23:50:34
1、选择题 下列关于右图装置的说法正确的是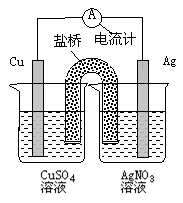
A.银电极是负极
B.铜电极上发生的反应为Cu-2e-=Cu2+
C.外电路中的电子是从银电极流向铜电极。
D.该装置能将电能转化为化学能
参考答案:B
本题解析:A项:银电极是正极,故错;C项:外路电子从铜电极流向银电极,故错;D项:原电池装置,化学能转化为电能,故错。故选B。
点评:本题考查学生原电池的工作原理,注意教材知识的灵活应用,属于基础知识的综合考查,难度不大。
本题难度:简单
2、填空题 (10分)图示的四个容器中分别盛有不同的溶液,除A、B外,其余电极均为石墨电极。甲为铅蓄电池,其工作原理为:Pb+PbO2+2H2SO4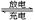 2PbSO4+2H2O,其两个电极的电极材料分别是PbO2和Pb。
2PbSO4+2H2O,其两个电极的电极材料分别是PbO2和Pb。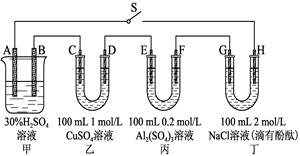
闭合S,发现G电极附近的溶液变红,20 min后,将S断开,此时C、D两极上产生的气体体积相同;据此回答:
(1)A电极的电极材料是______________(填“PbO2”或“Pb”)。
(2)电解后,要使丙中溶液恢复到原来的浓度,需加入的物质是________(填化学式)。
(3)到20 min时,电路中通过电子的物质的量为________。
(4)0~20 min,H电极上发生反应的电极反应式为______________
参考答案:28(1)PbO2 (2) H2O (3)0.4mol; (4)2Cl--2e-=Cl2↑;4OH--4e-=O2+2H2O
本题解析:(1)闭合S,发现G电极附近的溶液变红,说明G的电极反应为2H2O+2e-=H2+2OH-,G为阴极,则H为阳极,A为正极,A电极的电极材料是PbO2;(2)丙中电解硫酸铝溶液,实际上是电解水,要使丙中溶液恢复到原来的浓度,需加入的物质是水;(3)20 min后,将S断开,此时C、D两极上产生的气体体积相同,设C、D产生气体的物质的量为xmol,
C极发生的电极反应为Cu2+ + 2e- =" Cu" 、2H+ + 2e- = H2↑,D极的电极反应为4OH― - 4e- = 2H2O + O2↑
0.1 0.2 2x x 4x x
0.2+2x="4x" 解得x="0.1" 则到20 min时,电路中通过电子的物质的量为0.4mol;
(4)0~20 min,H电极上发生反应的电极反应式为2Cl--2e-=Cl2↑;0.2moLCl-只放电0.2moL,随后是OH-放电,即4OH--4e-=O2+2H2O 。
考点:考查铅蓄电池,电解原理的应用。
本题难度:一般
3、简答题 (14分)目前“低碳经济”备受关注。CO2的产生及有效开发利用成为科学家研究的重要课题。试利用所学知识,解决下列问题。
目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题.试运用所学知识,解决下列问题:
(1)已知某反应的平衡表达式为: 它所对应的化学反应为:_________________
它所对应的化学反应为:_________________
(2)一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生(1)中反应:其相关数据如表所示:
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需的时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3 |
参考答案:
本题解析:
本题难度:困难
4、选择题 用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如图所示(a,b为石墨电极)。下列说法中正确的是(?)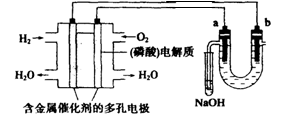
A.电池工作时,正极反应式为:O2+2H2O+4e- ="==" 4OH-
B.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
C.电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者
D.当电池中消耗0.02gH2时,a极周围会产生0.02gH2
参考答案:C
本题解析:左侧是原电池,右侧是电解池。在原电池电解质是酸性溶液,所以正极反应式为O2+4H++4e- ="==" 2H2O。电子只能通过导线传递,而不能通过溶液传递。a极是阳极,OH-放电生成氧气,所以正确的答案是C。
本题难度:一般
5、选择题 下图装置为一种可充电电池的示意图,其中的离子交换膜只允许K+通过,该电池充、放电的化学方程式为:2K2S2+KI3 K2S4+3KI。装置(Ⅱ)为电解池的示意图。当闭合开关K时,X附近溶液先变红。则下列说法正确的是
K2S4+3KI。装置(Ⅱ)为电解池的示意图。当闭合开关K时,X附近溶液先变红。则下列说法正确的是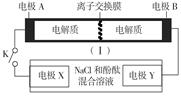
A.闭合K时,K+从右到左通过离子交换膜
B.闭合K时,A的电极反应式为:3I--2e-=I
C.闭合K时,X的电极反应式为:2Cl--2e-=Cl2↑(Ⅱ)
D.闭合K时,当有0.1 mol K+通过离子交换膜,X电极上产生标准状况下气体1.12 L
参考答案:D
本题解析:略
本题难度:简单