ʱ��:2019-07-03 23:49:00
1������� ��14�֣�
��1����ˮ��c(H��)��5.0��10��7mol/L�����ʱ��ˮ�е�c(OH��)�� ��
���¶Ȳ��䣬����ϡ����ʹc(H��)��5.0��10��3mol/L����c(OH��)�� ��
��2����CH3COONa����Һ�У������ӵ����ʵ���Ũ���ɴ�С��˳���� ��
��3��������ˮ��Һ�����ԣ���ԭ���ǣ������ӷ���ʽ��ʾ�� ��
��4����25�桢101kPa�£�0.5mol�ļ״���CH3OH����ȫȼ������CO2��Һ̬ˮʱ�ų�352kJ�����������ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽΪ ��
��5��1L 1 mol��L��1 H2SO4��Һ��2L 1 mol��L��1 NaOH��Һ��ȫ��Ӧ���ų�114.6kJ���������ʾ�к��ȵ��Ȼ�ѧ����ʽΪ ��
��6����֪����N2(g)+2O2(g)��2NO2(g) ��H��+67.7 kJ/mol ��
��N2H4(g)+O2(g)��N2(g)+2H2O(g) ��H����534 kJ/mol
��N2H4��NO2����ȫ��Ӧ���ɵ�������̬ˮ���Ȼ�ѧ����ʽΪ ��
�ο��𰸣���1��5.0��10-7mol/L (2��) 5.0��10-11mol/L(2��)
��2��c( Na+) > c(CH3COO��) > c( OH��)> c(H+)��2�֣���
��3��Al3+ + 3H2O  Al(OH)3 + 3H+�����֣� Al(OH)3��
Al(OH)3 + 3H+�����֣� Al(OH)3��
��4��CH3OH (l)��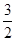 O2 (g) ��CO2 (g)��2H2O (l) ��H����704 kJ��mol-1
O2 (g) ��CO2 (g)��2H2O (l) ��H����704 kJ��mol-1
��5��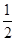 H2SO4(aq)��NaOH(aq)��
H2SO4(aq)��NaOH(aq)��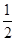 Na2SO4(aq)��H2O(l) ��H����57.3 kJ��mol-1�����֣�
Na2SO4(aq)��H2O(l) ��H����57.3 kJ��mol-1�����֣�
��6��2 N2H4 (g) + 2NO2 (g) �� 3N2 (g) + 4H2O (g) ��H����1135.7 kJ��mol-1 �����֣�
���2N2H4 (g) + NO2 (g) ��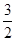 N2 (g) + ��H2O (g) ��H����567.85 kJ��mol-1
N2 (g) + ��H2O (g) ��H����567.85 kJ��mol-1
�����������1���ڴ�ˮ�д��ڵ���ƽ�⣺H2O H����OH��,��ˮ��c(H��)��5.0��10��7mol/L�����ʱ��ˮ�е�c(OH��)��5.0��10��7mol/L. Kw=2.5��10��13;���¶Ȳ��䣬����ϡ����ʹc(H��)��5.0��10��3mol/L����c(OH��)��Kw��c(H��)��2.5��10��13��5.0��10��3=5.0��10��11mol/L����2����CH3COONa����Һ�У�����CH3COO��ˮ�����ģ�����c( Na+) > c(CH3COO��)��ˮ������ˮ���������H+���ƻ���ˮ�ĵ���ƽ�⣬����ʹ��Һ�е�OH-��Ũ�ȴ���H+��Ũ�ȣ�c( OH��)> c(H+)�������ε�ˮ��̶������ģ��ε������������Ũ��Զ����ˮ������������ӵ�Ũ�ȣ�����c(CH3COO��) > c( OH��) c(H+)���ʸ����ӵ����ʵ���Ũ���ɴ�С��˳����c( Na+) > c(CH3COO��) > c( OH��)> c(H+)����3��������ˮ��Һ�����ԣ���ԭ����Al3+ + 3H2O
H����OH��,��ˮ��c(H��)��5.0��10��7mol/L�����ʱ��ˮ�е�c(OH��)��5.0��10��7mol/L. Kw=2.5��10��13;���¶Ȳ��䣬����ϡ����ʹc(H��)��5.0��10��3mol/L����c(OH��)��Kw��c(H��)��2.5��10��13��5.0��10��3=5.0��10��11mol/L����2����CH3COONa����Һ�У�����CH3COO��ˮ�����ģ�����c( Na+) > c(CH3COO��)��ˮ������ˮ���������H+���ƻ���ˮ�ĵ���ƽ�⣬����ʹ��Һ�е�OH-��Ũ�ȴ���H+��Ũ�ȣ�c( OH��)> c(H+)�������ε�ˮ��̶������ģ��ε������������Ũ��Զ����ˮ������������ӵ�Ũ�ȣ�����c(CH3COO��) > c( OH��) c(H+)���ʸ����ӵ����ʵ���Ũ���ɴ�С��˳����c( Na+) > c(CH3COO��) > c( OH��)> c(H+)����3��������ˮ��Һ�����ԣ���ԭ����Al3+ + 3H2O  Al(OH)3 + 3H+����4��ȼ������1mol�Ŀ�ȼ����ȫȼ�ղ����ȶ���������ʱ���ų�����������������ɵü״�ȼ���ȵ��Ȼ�ѧ����ʽΪCH3OH (l)��
Al(OH)3 + 3H+����4��ȼ������1mol�Ŀ�ȼ����ȫȼ�ղ����ȶ���������ʱ���ų�����������������ɵü״�ȼ���ȵ��Ȼ�ѧ����ʽΪCH3OH (l)��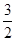 O2 (g)��CO2 (g)��2H2O (l) ��H����704 kJ��mol-1����5���к����������кͷ�Ӧ����1mol��ˮʱ���ų�������������1L 1 mol��L��1 H2SO4��Һ��2L 1 mol��L��1 NaOH��Һ��ȫ��Ӧ���ų�114.6kJ���������ʾ�к��ȵ��Ȼ�ѧ����ʽΪ
O2 (g)��CO2 (g)��2H2O (l) ��H����704 kJ��mol-1����5���к����������кͷ�Ӧ����1mol��ˮʱ���ų�������������1L 1 mol��L��1 H2SO4��Һ��2L 1 mol��L��1 NaOH��Һ��ȫ��Ӧ���ų�114.6kJ���������ʾ�к��ȵ��Ȼ�ѧ����ʽΪ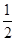 H2SO4(aq)��NaOH(aq)��
H2SO4(aq)��NaOH(aq)��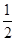 Na2SO4(aq)��H2O(l) ��H����57.3 kJ��mol-1����6���ڡ�2���٣������ɵ�2 N2H4 (g) + 2NO2 (g) �� 3N2 (g) + 4H2O (g) ��H����1135.7 kJ��mol-1��дΪ2N2H4 (g) + NO2 (g) ��
Na2SO4(aq)��H2O(l) ��H����57.3 kJ��mol-1����6���ڡ�2���٣������ɵ�2 N2H4 (g) + 2NO2 (g) �� 3N2 (g) + 4H2O (g) ��H����1135.7 kJ��mol-1��дΪ2N2H4 (g) + NO2 (g) ��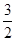 N2 (g) + ��H2O (g) ��H����567.85 kJ��mol-1��
N2 (g) + ��H2O (g) ��H����567.85 kJ��mol-1��
���㣺����������ʵĵ��롢ˮ�����ӻ��������ε�ˮ�⡢��˹���ɵ�Ӧ�á�����Ũ�ȱȽϡ��к��ȡ�ȼ���ȵ��Ȼ�ѧ����ʽ����д��֪ʶ��
�����Ѷȣ�һ��
2��ѡ���� ����ˮ������ӷ���ʽ��ȷ����
[? ]
A��Fe3++3H2O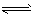 Fe(OH)3��+3H+
Fe(OH)3��+3H+
B��Br-+H2O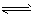 HBr+OH-
HBr+OH-
C��CO32-+H2O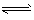 H2CO3+2OH-
H2CO3+2OH-
D��NH4++ H2O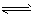 NH3��H2O +H+
NH3��H2O +H+
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3��ѡ���� Ҫ��ȥMgCl2������Һ��������FeCl3������ѡ�õ��Լ���
A��MgO
B��MgCO3
C��NaOH
D��Mg(OH)2
�ο��𰸣�C
�����������pH���ڵ�3���ҡ���ʹ��NaOH��pH���ߵ���þ���ӳ�����
�����Ѷȣ���
4������� �����仯����������������й㷺Ӧ�á���ش��������⣺
��1��������FeS2�������������ұ����������Ҫԭ�ϡ�����һ����ӦΪ3FeS2+8O2 Fe3O4+6SO2����3mol FeS2�μӷ�Ӧ��ת�� mol���ӡ�
Fe3O4+6SO2����3mol FeS2�μӷ�Ӧ��ת�� mol���ӡ�
��2��FeCl3��Һ������ӡˢ��·ͭ�帯ʴ������Ӧ�����ӷ���ʽΪ ���Ӹ�ʴ��Һ���յõ�����ͭ������Ҫ���Լ��� ��
��3�����������ƣ�Fe2(SO4)3Ҳ��������ˮ������ʹ��ʱ����Fe2(SO4)3������ʹ���Է�ˮ�е������������ȥ����ԭ���� ��
��4�������ĵ绯ѧ��ʴ��ʾ��ͼ���£�����ͼ�����ļ��ɳ�Ϊ�����绯ѧ�����ļ�ʾ��ͼ��������ͼ���߿��������ģ����ü�ͷ������������ķ���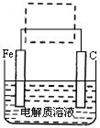
�ο��𰸣���1��32
��2��2Fe3++Cu=2Fe2++Cu2+ ���ۡ�ϡ����
��3�����Է�ˮ����Fe3+ ��ˮ�⣬ʹ�䲻���������������õ�Fe(OH)3����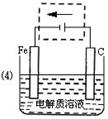
�����������1����Ӧ��FeS2��������Ļ��ϼ۾����ߣ��������ϼ��½������Ը��ݻ��ϼ���������Ҳ���Ը��ݻ��ϼ۽�����������ת�Ƶ�������3mol FeS2�μӷ�Ӧ��ת�Ƶ�����Ϊ8��4=32mol����2���Ӹ�ʴҺ�л���ͭӦ�����û��������������û�������ϡ�����ȥͭ�е�������3��Fe2(SO4)3��������ˮ������Դ����ˮ����������������壬�����Է�ˮ����Fe3+ ��ˮ�⣬ʹ�䲻���������������õ�Fe(OH)3���壬�ʲ��ܳ�ȥ�������4����ͼ��ʾ���ĵ绯ѧ����ӦΪ������ӵ�Դ�ĵ绯ѧ��������Ӧ���Դ�ĸ���������
���㣺���黯ѧԭ����������ԭ��Ӧ���绯ѧ��ˮ����й����⡣
�����Ѷȣ�����
5��ѡ���� ����0.1mol�BL-1?Na2CO3��Һ,����˵����ȷ����
A.�����¶ȣ���Һ��pH����
B.c��Na+��=2c��CO32-��+ c��HCO3-��+ c��H2CO3��
C.c��Na+��+c��H+��= 2? c��CO32-��+ 2c��HCO3-��+ c��OH-��
D.��������NaOH���壬c��CO32-����c��Na+��������
�ο��𰸣�D
���������̼����ˮ���Լ��ԣ�ˮ�����ȣ������¶ȣ��ٽ�ˮ�⣬pH����A����ȷ��B����ȷ�������������غ㣬Ӧ����c��Na+��=c��CO32-��+ c��HCO3-��+ c��H2CO3����C����ȷ��Ӧ����c��Na+��+c��H+��= 2? c��CO32-��+ c��HCO3-��+ c��OH-��������������������ˮ�⣬c��CO32-����c��Na+��������D��ȷ����ѡD��
�����Ѷȣ�һ��