时间:2019-07-03 23:26:09
1、选择题 能促进水的电离,并使溶液中c(H+)>c(OH-)的操作是(?)
①将水加热煮沸?②向水中投入一小块金属钠?③向水中通CO2
④向水中通NH3?⑤向水中加入明矾晶体?⑥向水中加入NaHCO3固体
⑦向水中加NaHSO4固体
A.①③⑥⑦
B.①③⑤⑥
C.⑤⑦
D.⑤
2、选择题 pH=11的X、Y两种碱溶液各10mL,分别稀释至1000mL。其pH与溶液体积(V)的关系如图所示,下列说法正确的是(?)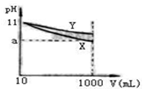
A.X、Y两种碱的物质的量浓度一定相等
B.稀释后,X溶液碱性比Y溶液碱性强
C.若9<a<11,则X、Y都是弱碱
D.完全中和X、Y两溶液时,消耗同浓度盐酸的体积VX>VY
3、选择题 关于常温下pH=2的醋酸溶液,下列叙述正确的是
A.c(CH3COOH)=0.01mol·L-1
B.c(H+)=c(CH3COO-)
C.加水稀释100倍后,溶液pH=4
D.醋酸的电离常数为Ka,CH3COO-的水解常数为Kh,则Ka·Kh=Kw
4、选择题 下列说法正确的是(?)
A.pH=2和pH=l的硝酸中c(H+)之比为10:1
B.一元酸与一元碱恰好完全反应后的溶液中一定存在c(H+)=c(OH-)
C.KAl(SO4)2溶液中离子浓度的大小顺序为c(SO2-4)>c(K+)>c(Al3+)>c(H+)>c(OH-)
D.常温下,将pH均为12的氨水和NaOH溶液分别加水稀释100倍后,NaOH溶液的pH较大
5、实验题 (12分)某学生用0.l000mol.L-l盐酸标准溶液测定某烧碱样品的纯度(杂质不与盐酸反应)。实验步骤如下:
(1)配制待测液:用2.50 g含有少量杂质的固体烧碱样品配制500 mL溶液。需用的玻璃仪器除了烧杯、胶头滴管、玻璃棒外,还需要??。
(2)滴定:
I.用蒸馏水洗涤酸式滴定管,并立即注入盐酸标准溶液至“O”刻度线以上
Ⅱ.固定好滴定管并使滴定管尖嘴充满液体,调节液面至“0”或“O”刻度线以下,并记录读数
Ⅲ.移取20.OOmL待测液注入洁净的锥形瓶中,并加入2滴酚酞试 液
Ⅳ.用标准液滴定至终点,记录滴定管液面读数。
①上述滴定步骤中有错误的是(填编号)?,该错误操作会导致测定结果?(填“偏大”、“偏小”或“无影响”)。
②步骤Ⅳ中滴定时眼睛应?:判断滴定终点的现象是?。
③若步骤II中仰视读数,步骤Ⅳ中俯视读数,则会使测定结果?(填“偏大”、“偏小”或“无影响’")。
(3)按正确操作测得有关数据记录如下:
| ? 滴定次数 | ? 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 20.38 |
| 第二次 | 20.00 | 4.00 | 24.20 |
| 第三次 | 20.00 | 2.38 | a |