时间:2019-07-03 23:20:20
1、填空题 已知H2A是一种无机二元酸,请回答以下问题:
(1) 若H2A为二元弱酸,在水溶液中的电离方程式为 ;
(2) 若NaHA溶液显碱性,则H2A是 (填“强酸”、“弱酸”或“无法确定”),原因是 。
(3) 若溶液显酸性,在25℃下,若向0.1 mol・L-1的NaHA溶液中逐滴滴加0.1 mol・L-1 KOH溶液至溶液呈中性。此时该混合溶液中下列关系中,一定正确的是 ;
a.c(H+)・c(OH-)=1×10-14 b.c(Na+)+c(K+)=0.1 mol・L-1
c.c(Na+)>c(K+) d.c(Na+)=c(HA-)+c(A2-)
参考答案:
(1)H2A H++HA-,HA-
H++HA-,HA- H++A2-(2分)
H++A2-(2分)
(2)弱酸(1分)HA-水解生成H2A和OH-使溶液显碱性,故H2A必为弱酸;(2分)
(3)a(2分) ;
本题解析:(1)多元弱酸部分电离,分步书写。(2)若NaHA溶液显碱性, 说明HA-水解生成H2A和OH-使溶液显碱性,故H2A必为弱酸;(3)在25℃下,任何溶液一定存在c(H+)・c(OH-)=1×10-14,故a正确;滴加到溶液刚好反应时,生成Na2A和K2A,溶液呈碱性,要成中性必须NaHA过量,故b错、C错;根据物料守恒:c(Na+)=c(HA-)+c(A2-)+ c(H2A),故d错。
考点:考查弱电解质的电离、盐类水解、水溶液中的离子平衡等相关知识。
本题难度:一般
2、填空题 (10分)
(1)Cu(NO3)2的水溶液呈 (填“酸”、“中”、“碱”)性,常温时的pH 7(填“>”、“=”、“<”),原因是(用离子方程式表示): ;实验室在配制AgNO3的溶液时,常将AgNO3固体先溶于较浓的硝酸中,然后再用蒸馏水稀释到所需的浓度,以 (填“促进”、“抑制”)其水解。
(2)氯化铝水溶液呈 性,原因是(用离子方程式表示):______ ,把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是 。
(3)在配制硫化钠溶液时,为了防止发生水解,可以加入少量的 。
参考答案:(10分)(1) 酸,<,Cu2++ H2O 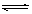 Cu(OH)2+ 2H+,抑制
Cu(OH)2+ 2H+,抑制
(2)酸,Al3++3H2O 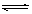 Al(OH)3+3H+, Al2O3 (3)NaOH
Al(OH)3+3H+, Al2O3 (3)NaOH
本题解析:(1)Cu(NO3)2是强酸弱碱盐,铜离子水解,水溶液呈酸性,pH小于7。水解方程式是Cu2++ H2O 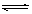 Cu(OH)2+ 2H+;硝酸银溶于水,银离子水解,溶液显酸性。所以将AgNO3固体先溶于较浓的硝酸中的目的是抑制银离子的水解。
Cu(OH)2+ 2H+;硝酸银溶于水,银离子水解,溶液显酸性。所以将AgNO3固体先溶于较浓的硝酸中的目的是抑制银离子的水解。
(2)氯化铝溶于水,铝离子水解,溶液显酸性,水解方程式是Al3++3H2O 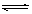 Al(OH)3+3H+。水解吸热,加热促进水解,且生成的氯化氢挥发,进一步促进水解,所以最终得到的是氢氧化铝,灼烧得到氧化铝。
Al(OH)3+3H+。水解吸热,加热促进水解,且生成的氯化氢挥发,进一步促进水解,所以最终得到的是氢氧化铝,灼烧得到氧化铝。
(3)硫化钠溶于水,硫离子水解,溶液显碱性。所以在配制硫化钠溶液时,为了防止发生水解,可以加入少量的氢氧化钠。
考点;考查盐类水解的应用
点评:盐电离出来的离子结合水电离出来的 H+或 OH-生成弱电解质的过程。盐类水解的应用主要有:①判断盐溶液的酸碱性和比较盐溶液酸碱性的强弱时,通常需考虑盐的水解。②比较盐溶液中各离子浓度的相对大小时,当盐中含有易水解的离子,需考虑盐的水解。③判断溶液中离子能否大量共存。当有弱碱阳离子和弱酸阴离子之间能发生强烈双水解,则不能在溶液中大量共存。④配制易水解的盐溶液时,需考虑抑制盐的水解。⑤选择制备盐的途径时,需考虑盐的水解。⑥离子除杂、化肥的使用需考虑盐类的水解。⑦溶液中离子浓度大小比较时需要考虑盐类水解。
本题难度:一般
3、选择题 常温下,体积、物质的量浓度均相等的四种溶液:
①盐酸;②醋酸;③氨水;④CH3COONa溶液。下列说法正确的是
A.将①与②分别稀释相同倍数后溶液的pH:①>②
B.若②与③混合后溶液呈中性,则在常温下Ka(CH3COOH)=Kb(NH3?H2O)
C.③与④中已电离的水分子的数目相等
D.②与④混合所得溶液显酸性,则:c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
参考答案:B
本题解析:A、体积、物质的量浓度均相等的①与②,因盐酸完全电离,醋酸是弱酸,电离程度较小,pH:①<②,再稀释相同的倍数,仍然是①<②,故A错误;②与③混合后生成醋酸铵溶液,铵根离子和醋酸根离子均发生水解,溶液显中性,说明两者的水解能力相同,故Ka(CH3COOH)=Kb(NH3?H2O),B正确;C、氨水抑制水的电离,醋酸钠溶液中醋酸根离子水解,促进水的电离,故C错误;醋酸和醋酸钠组成的混合溶液显酸性,说明醋酸根离子的水解程度小于醋酸的电离程度,醋酸分子的浓度小于钠离子的浓度,根据电荷守恒可得c(CH3COO-)+c(OH-)=c(Na+)+c(H+),故c(CH3COO-)+c(OH-)>c(CH3COOH)+c(H+),D错误;故选B。
考点:考查了强弱电解质的电离、盐水解的实质、离子浓度的比较等知识。
本题难度:一般
4、选择题 将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合后,溶液pH>7,以下关系式错误的是A.c(A-)> c(HA) B.c(Na+)+c(H+)= c(A-)+c(Cl-)+c(OH-)
C.c(HA)+c(A-)=0.1mol/L D.c(Na+)= c(A-)+ c(HA)
参考答案:A
本题解析:将0.2 mol/L NaA溶液和0.1 mol/L盐酸等体积混合,发生反应:NaA+HCl=NaCl+HA。得到的是NaA、NaCl、HA等浓度等体积的混合溶液。由于此时溶液pH>7,说明NaA的水解作用大于HA的电离作用。所以c(A-)< c(HA)。A错误。根据电荷守恒可得c(Na+)+c(H+)= c(A-)+c(Cl-)+c(OH-)。正确。根据物料守恒可得c(HA)+c(A-)=0.1mol/L。正确。由于在物质NaA中n(Na+)=n(A-).A-在溶液中与酸发生反应变为HA。所以根据物料守恒及原子守恒可得c(Na+)= c(A-)+ c(HA)。正确。
考点:考查混合溶液中离子浓度的大小比较的知识。
本题难度:一般
5、选择题 下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/c(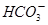 )的值保持增大
)的值保持增大
②浓度均为0.1mol・L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c( )+c(
)+c(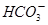 )]
)]
③在0.1mol・L-1氨水中滴加0.1mol・L-1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=10-a mol・L-1
④向0.1mol・L-1(NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c( )、c(
)、c( )均增大
)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+2c(H2S)+c(HS-)
A.①④
B.②④
C.①③
D.②⑤
参考答案:B
本题解析:①加水稀释,碳酸氢根的水解程度增大,所以比值增大,正确;②在同业中遵循物料守恒,钠原子:碳原子=3:2,所以有2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],错误;③恰好完全反应时,溶液中的氢离子和氢氧根离子都是水电离的,所以溶液的pH=a,则溶液中的氢离子浓度=10-amol/L,则氢氧根离子浓度也为10-amol/L,正确;④加入氢氧化钠固体,促进铵根离子水解,抑制亚硫酸根离子水解,所以铵根离子浓度减小,亚硫酸根离子浓度增大,错误;⑤根据溶液中质子守恒,即水电离的氢离子和氢氧根离子浓度永远相等,可以写出c(H+)=c(OH-)+2c(H2S)+c(HS-),正确;所以选B。
考点:溶液的酸碱性和溶液中的离子浓度比较
本题难度:困难