时间:2019-07-03 23:05:49
1、选择题 下列有关说法正确的是
A.常温下,0.1 mol・L-1 CH3COOH溶液的pH=1
B.铅蓄电池在放电过程中,负极质量增加,正极pH减少
C.反应CO2(g)+C(s)=2CO(g)在低温下不能自发进行,则其△H>0
D.常温下,向AgCl浊液中加入少量NaCl饱和溶液,则c(Ag+)、Ksp(AgCl)均减小
2、填空题 (1) 25℃时,部分弱酸的电离平衡常数如下表:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | Ki=1.7×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
3、选择题 当将金属钠溶解在液氨中时,能形成一种蓝色的液氨溶液,蓝色据认为是生成了电子氨化物e(NH3)n-的缘故,其生成可用以下的反应式表示:Na+nNH3=Na++e(NH3)n-,小心蒸去氨气可得白色固体NaNH2,而且有以下反应发生:2Na+2NH3=2NaNH2+H2,下列说法不正确的是
[? ]
A.液氨不能发生电离
B.液氨能电离出NH4+和NH2-
C.金属钠的液氨溶液时发生了氧化还原反应
D.金属钠的液氨溶液时蓝色会逐渐褪去
4、选择题 液氨与水的电离相似,存在关微弱的电离:2NH3+NH3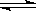 NH4++NH2―。对该体系的说法中错误的是?(?)
NH4++NH2―。对该体系的说法中错误的是?(?)
A.液氨中c(NH4+)与c(NH2―)的乘积为一常数
B.液氨电离达到平衡时,c(NH3)=c(NH4+)=c(NH2―)
C.只要不加入其它物质c(NH4+)=c(NH2―)
D.液氨中存在NH3、NH4+、NH2―、H2O、NH3 ・H2O等粒子。
・H2O等粒子。
5、选择题 下列说法错误的是( )
A.常温下,将pH=3的醋酸溶液稀释到原体积的10倍后,溶液的pH小于4
B.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH.若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸
C.用0.200mol?L-1NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1mol?L-1),至中性时,溶液中的酸未被完全中和
D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、②0.1mol?L-1盐酸、③0.1mol?L-1氯化镁溶液、④0.1mol?L-1硝酸银溶液中,Ag+浓度:④>①>②>③