时间:2019-06-28 22:12:25
1、实验题 (16分)已知硫酸亚铁铵晶体为浅绿色,易溶于水、不溶于乙醇,在水中的溶解度比FeSO4和(NH4)2SO4都要小;能水解;具有还原性,但比硫酸亚铁稳定。
以下是将绿矾(FeSO4?7H2O)、硫酸铵以相等物质的量混合可制得摩尔盐晶体的流程图。根据下图回答: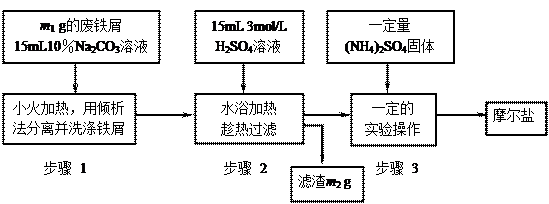
(1)为处理废铁屑表面的油污,用10%Na2CO3溶液清洗,请用离子方程式表示Na2CO3溶液呈碱性的原因:? ▲?。
(2)步骤1中采用倾析法分离出铁屑,下列适合用倾析法的有? ▲?:
A.沉淀的颗粒较大? B.沉淀容易沉降? C.沉淀呈胶状? D.沉淀呈絮状
(3)步骤2 中铁屑过量的目的是(用离子方程式表示):?▲?。步骤2中溶液趁热过滤的原因是? ▲?。
中铁屑过量的目的是(用离子方程式表示):?▲?。步骤2中溶液趁热过滤的原因是? ▲?。
(4)步骤3中,加入(NH4)2SO4固体后,应 加热到? ▲?时,停止加热。需经过的实验操作包括:? ▲?、 ▲ 、减压过滤(或抽滤)等得到较为? ▲?的晶体。
加热到? ▲?时,停止加热。需经过的实验操作包括:? ▲?、 ▲ 、减压过滤(或抽滤)等得到较为? ▲?的晶体。
(5)抽滤装置的仪器有:? ▲?、? ▲?、安全瓶、抽气泵组成。
(6)产品中Fe2+的定量分析:
制得的摩尔盐样品中往往含有极少量的Fe3+。为了测定摩尔盐产品中Fe2+的含 量,一般采用在酸性下用KMnO4标准液滴定的方法。
量,一般采用在酸性下用KMnO4标准液滴定的方法。
称取4.0 g的摩尔盐样品,溶于水,并加入适量稀硫酸。用0.2 mo1/L KMnO4溶液滴定,当溶液中Fe2+全部被氧化时,消耗KMnO4溶液体积 10.00 mL。
①请完成滴定过程中发生的离子方程式:
?Fe2++?MnO4-+(? )="?" ?Mn2++?Fe3++?H2O
②本实验的指示剂? ▲?。
A.酚酞? B.甲基橙? C.石蕊? D.不需要
③KMnO4溶液置于? ▲? (酸式、碱式)滴定管中
④终点颜色的变化:? ▲?。
⑤产品中Fe2+的质量分数为? ▲?。 (7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为:? ▲?。(用a,b,c回答)
(7)在25℃时,相同物质的量浓度的(NH4)2 CO3、(NH4)2SO4、摩尔盐三种盐溶液a,b,c,其铵根离子浓度由小到大的排列顺序为:? ▲?。(用a,b,c回答)
2、实验题 一包白色粉末中一定含有碳酸钠,可能还含有硫酸钠、氯化钠中的一种或两种,为进一步确认白色粉末的成份,某兴趣小组对白色粉末样品进行了探究。
可选用的仪器:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹
可选用的药品:1.0 mol·L-1H2SO4、1.0 mol·L-1HNO3、1.0mol·L-1HCl、NaOH稀溶液、0.1 mol·L-1AgNO3、0.1 mol·L-1BaCl2、0.1 mol·L-1Ba(NO3)2、蒸馏水。
(1)以下是实验探究过程:
1)提出假设:
假设1 白色粉末为___________的混合物;
假设2 白色粉末为___________的混合物;
假设3 白色粉末为碳酸钠、硫酸钠、氯化钠的混合物;
2)基于假设设计实验方案
3)根据实验方案进行实验
请回答:
(2)某同学取少许样品于试管中,加适量蒸馏水溶解,向试管中滴入0.1 mol·L-1的BaCl2溶液,有白色沉淀产生,他认为样品中含有Na2SO4。你认为他的结论是___________(填“对的”或“错的”),原因是:______________________。
(3)基于假设3,请根据实验方案,将实验操作和预期的现象及结论填入下表中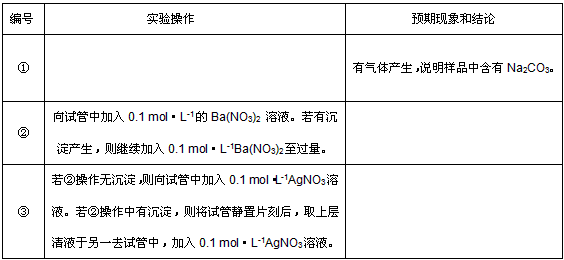
3、选择题 为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是 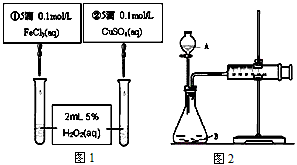
[? ]
A.图1实验可通过观察产生气泡快慢来比较反应速率的大小
B.若图1所示实验中反应速率为①>②,则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C.用图2装置测定反应速率,只测定反应产生的气体体积即可
D.为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
4、实验题 某化学兴趣小组参考工业制硝酸的化学原理,在实验室用下列各装置进行组合来制备硝酸并验证硝酸的性质(所给装置必须用到并且只能用一次,各装置中的试剂均足量。已知常温下CaCl2能吸收氨气)。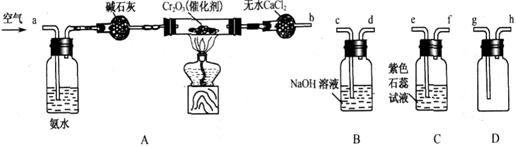
(1)装置的连接顺序为(用a、b、c、d等字母表示):b接(? ),(? )接(? ),(? )接(? )。
(2)写出氨气催化氧化的化学方程式______________________。
(3)进行实验时,装置A中碱石灰的作用是_____________;D中的现象是_______________。
(4)能证明有硝酸生成的现象是__________________________________________。
(5)实验开始时,下列操作顺序最合理的是______________。
a.先加热A装置中的催化剂.再由导管a通入空气
b.先由导管a通人空气,再加热A装置中的催化剂
c.在由导管a通人空气的同时,加热A装置中的催化剂
5、实验题 已知单质硫是淡黄色固体粉末,难溶于水。实验室制氯气的反应原理为:MnO2+4HCl(浓) ?MnCl2+Cl2↑+2H2O,为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:?
?MnCl2+Cl2↑+2H2O,为了验证氯元素的非金属性比硫元素的非金属性强,某化学实验小组设计了如下实验,请回答下列问题:? 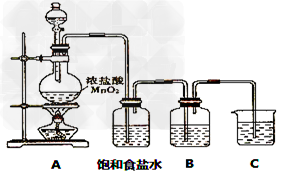
(1)已知:①硫酸比次氯酸稳定;②高氯酸比硫酸酸性强;③S2-比Cl-还原性强;④HCl比H2S稳定;⑤硫原子与氯原子电子层数相同,氯原子半径小于硫原子。可作为氯元素比硫元素非金属性强的依据的是______________?。
A.②④?B.②③④⑤?C.②④⑤?D.全部
(2)装有饱和食盐水的洗气瓶的作用是?______________
(3)装置B中盛放的试剂是______________(填选项),实验现象为____________?。
A.Na2S溶液?B.Na2SO3溶液?C.Na2SO4溶液
(4)装置B中的溶液在实验后质量增重了0.78g,则在B中反应的气体为___________mol
(5)装置C中盛放烧碱稀溶液,目的是吸收剩余气体,防止污染空气。写出反应的离子方程式:____________________。