时间:2019-06-28 22:04:08
1、填空题 (8分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。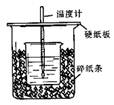
通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
(1)从实验装置上看,图中尚缺少的一种玻璃用品是 。
(2)烧杯间填满碎纸条的作用是 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值 (填“偏大、偏小、无影响”)
(4)如果用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量 (填“相等、不相等”),所求中和热 (填“相等、不相等”),简述理由
(5)用相同浓度和体积的氨水(NH3・H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
参考答案:17.(8分)(1)环形玻璃搅拌棒 (2)减少实验过程中的热量损失。 (3)偏小
(4)不相等;相等;因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关
(5)偏小;
本题解析:(1)根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,答案为:环形玻璃搅拌器;(2)中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是:减少实验过程中的热量损失,答案为:减少实验过程中的热量损失;(3)大烧杯上如不盖硬纸板,会导致热量散失,求得的中和热数值偏小;(4)反应放出的热量和所用酸以及碱的量的多少有关,若用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,生成水的量增多,所放出的热量偏高,但是中和热的均是强酸和强碱反应生成1mol水时放出的热,与酸碱的用量无关,所以用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液反应,测得中和热数值相等,答案为:不相等;相等;因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关;(5)氨水为弱碱,电离过程为吸热过程,所以氨水代替NaOH溶液反应,反应放出的热量小于57.3kJ,答案为:偏小.
考点:考查中和热的测定。
本题难度:一般
2、选择题 根据化学反应的实质是旧键断裂新键形成这一现实,下列变化不属于化学反应的是( )
A.白磷在260℃时转化为红磷
B.石墨在高温下转化为金刚石
C.NaCl熔化
D.五氧化二磷吸水
参考答案:A、白磷在260℃时转化为红磷,既有旧化学键断裂,又有新化学键形成,故A不选;
B、石墨在高温下转化为金刚石,既有旧化学键断裂,又有新化学键形成,故B不选;
C、NaCl熔化属于物理过程,只存在旧键的断裂,没有新键生成,故C选;
D、五氧化二磷吸水生成磷酸,既有旧化学键断裂,又有新化学键形成,故D不选;
故选:C.
本题解析:
本题难度:一般
3、填空题 ①Ar ②CO2 ③KCl ?④NaOH四种物质中,只存在共价键的是?,(填序号,下同)只存在离子键的是?,既存在离子键,又存在共价键的是?,不存在化学键的是?。
参考答案:②;③;④;①
本题解析:考查化学键的判断。一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间形成共价键。稀有气体元素的最外层电子已经达到稳定结构,所以稀有气体分子中不存在化学键。
本题难度:一般
4、选择 题 下列离子方程式表达正确的是
A.SO2通入溴水中溴水褪色:SO2+2H2O+Br2=2H++SO42-+2HBr
B.漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3-
C.NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O
D.Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O
参考答案:C
本题解析:分析:A、HBr为强电解质,在水中完全电离;
B、漂白粉溶液在空气中失效应生成碳酸钙和次氯酸;
C、溶液呈中性时,氢离子与氢氧根离子恰好完全反应,则NaHSO4与Ba(OH)2物质的量之比为2:1;
D、Fe(OH)3溶于氢碘酸中应发生氧化还原反应.
解答:A、因HBr为强电解质,则正确的离子反应为SO2+2H2O+Br2=4H++SO42-+2Br-,故A错误;
B、漂白粉溶液在空气中失效应生成碳酸钙和次氯酸,则正确的离子反应为Ca2++2ClO-+CO2+H2O=2HClO+CaCO3↓,故B错误;
C、硫酸氢钠溶液中滴加氢氧化钡至中性时,硫酸氢钠与氢氧化钡的物质的量之比为2:1,其反应为2NaHSO4+Ba(OH)2=2H2O+Na2SO4+BaSO4↓,
离子反应为2H++SO42-+Ba2++2OH-=2H2O+BaSO4↓,故C正确;
D、因铁离子具有氧化性,氢碘酸具有还原性,则正确的离子反应为2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,明确反应的实质是解答的关键,并注意强电解质的判断、溶液为中性、离子之间的氧化还原反应来解答即可.
本题难度:简单
5、选择题 热化学方程式中化学式前的化学计量数表示( )
A.分子个数
B.原子个数
C.物质的质量
D.物质的量
参考答案:D
本题解析:热化学方程式中化学式前的化学计量数表示参加反应的物质的物质的量,答案选D。
本题难度:一般