ʱ��:2019-06-28 21:20:47
1��ѡ���� ���ж��ڡ�Ħ������������ȷ����?��?��
A��Ħ���ǹ��ʵ�λ�Ƶ��߸�������֮һ
B��Ħ�������ʵ����ĵ�λ�����Ħ������Ϊmol
C��Ħ���DZ�ʾ���������ĵ�λ
D��1mol����6.02��1023��O2
�ο��𰸣�C
�����������
�����Ѷȣ���
2��ѡ���� �������ܱ������зֱ����Ne��H2��O2�������壬�����ǵ��¶Ⱥ��ܶȶ���ͬʱ�������������ѹǿ��p����С�������
A��p (Ne) < p (H2) < p (O2)
B��p (H2) < p (O2) < p (Ne)
C��p (O2) < p (Ne) < p (H2)
D��p (H2) < p (Ne) < p (O2)
�ο��𰸣�C
������������ݰ����ӵ�����֪�����¶Ⱥ��ܶȶ���ͬ�����£�ѹǿ��Ħ�������ʷ��ȡ�Ne��Ħ������Ϊ20g/mol��H2��Ħ������Ϊ2g/mol��O2��Ħ������Ϊ32g/mol���������������ѹǿ��p���Ӵ�С��˳����p��H2����p��Ne����p��O2����ѡC��
���㣺���鰢���ӵ����ɵ�Ӧ�á�
�����Ѷȣ�һ��
3��ѡ���� Mg��Zn��Al���ֽ����Ļ������������ϡ���ᷴӦ������2.8��������S��T��P����ԭ���ֽ��������ʵ���֮�Ϳ����ǣ� ��
A��0.125 mol
B��0.10 mol
C��0.08 mol
D��0.20 mol
�ο��𰸣�B
���������
��״����Ϊ2.8L��������ʵ���Ϊ2.8L/22.4L��mol��1=0.125mol��
����Mg��Zn�����ᷴӦ������Ϊ+2�ۣ�AlΪ+3�ۣ����õ���ת���غ�������ֽ�����������֮�ͣ�
����2n��Mg��+2n��Zn��+3n��Al��=2n��H2����
��n��Mg��+n��Zn��+1.5n��Al��=n��H2��=0.125mol��
0.125mol =n��Mg��+n��Zn��+1.5n��Al��> n��Mg��+n��Zn��+n��Al��
��ȫ��Al���������СΪ��0.125mol��2/3=0.0833mol��
��ѡB��
�����Ѷȣ�һ��
4������� �ڱ�״���£�������N2��O2�������ԼΪ4��1����N2��O2�����ʵ���֮��Ϊ_________���������ܶ�ԼΪ_________��������ƽ����Է�������Ϊ_________��
�ο��𰸣�4��1? 1.29 g��L-1? 29
���������ͬ�¡�ͬѹ�£�������������֮�ȵ������ǵķ����������ʵ���֮�ȣ�����N2��O2�����ʵ���֮��Ϊ4��1����n(N2)="4" mol��n(O2)="1" mol����V="(1+4)mol��22.4" L��mol-1="112" L��
���Կ������ܶȣ�
��=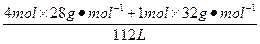 ��1.29 g��L-1
��1.29 g��L-1
��ƽ��Ħ������ ��29 g��mol-1
��29 g��mol-1
�����Ѷȣ���
5��ѡ���� ��20��ʱһ���������ڲ���һ��©���ҿɻ����Ļ����������ָ������������ҡ����ҳ���N2�����ҳ���H2��O2����������ͣ�������1/5��������ͼa��Ȼ���ȼ����H2��O2�����������������������©�������ָ���ԭ���¶ȣ�����ǡ��ͣ���м䣨����ͼb����ˮ����������ɺ��ԣ���ӦǰH2��O2������ȿ�����(? )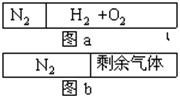
A��1�U1
B��1�U3
C��7�U1
D��5�U1
�ο��𰸣�A
�������������ѹǿ��ȣ���������ʵ���֮�ȵ������֮�ȣ��赪�������ʵ���Ϊ1mol����H2��O2�����ʵ���Ϊ4mol����Ӧ���������ͣ�����������м䣮˵����Ӧ��������������ʵ�����ȣ���������ʣ������1mol����Ӧ��H2��O2��3mol������2H2+O2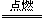 2H2O����֪��Ӧ��O2Ϊ1mol����Ӧ��H2Ϊ2mol����ʣ�������ΪH2����ӦǰH2Ϊ3mol��O2Ϊ1mol����ӦǰH2��O2�������Ϊ3��1����ʣ�������Ϊo2����ӦǰH2Ϊ2mol��O2Ϊ2mol����ӦǰH2��O2�������Ϊ1��1����A����ȷ��
2H2O����֪��Ӧ��O2Ϊ1mol����Ӧ��H2Ϊ2mol����ʣ�������ΪH2����ӦǰH2Ϊ3mol��O2Ϊ1mol����ӦǰH2��O2�������Ϊ3��1����ʣ�������Ϊo2����ӦǰH2Ϊ2mol��O2Ϊ2mol����ӦǰH2��O2�������Ϊ1��1����A����ȷ��
�����Ѷȣ�һ��
1��ѡ���� ����������ȷ����
A����״���£�l mol�κ����ʵ������Ϊ22.4 L
B��CH4��Ħ������Ϊ16 g
C��1mol H2O������Ϊ18 g?mol����
D��3.01��l023��SO2���ӵ�����Ϊ32 g
2������� ��1��44.8Lij�����ڱ�״���µ�����Ϊ142g���������Ħ������Ϊ______��
��2��N2�ڱ�״���µ��ܶ�Ϊ______g/L��
��3����______molAL2��SO4��3�к�0.3molSO42-�����к�Al3+______����
3��ѡ���� V L��������Һ�к���Al3+mg������Һ��SO42�������ʵ���Ũ��Ϊ[? ]?
A��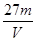 mol/L
mol/L
B��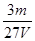 mol/L
mol/L
C��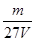 mol/L
mol/L
D��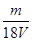 mol/L
mol/L
4��ѡ���� ����һ�����ʵ���Ũ�ȵ�NaOH��Һʱ�����������ҺŨ��ƫ�ߵ�ԭ���ǣ�������
A������NaOH������
B������ǰ��Һδ��ȴ
C������ʱ����λ�÷Ŵ�
D��������ƿ��ˮʱ�۾�һֱ����Һ��
5��ѡ���� ��NA��ʾ�����ӵ���������ֵ������˵��������ǣ�?��
A��1mol H2��O2�Ļ�������ڱ�״���µ����ԼΪ22.4L
B��20�桢101kPa�£�16g��������������ԭ����ΪNA
C��18gˮ�����ĵ�����Ϊ8NA
D���ڱ�״���£�0.5NA������������ռ���Լ��11.2L