时间:2019-06-28 20:07:51
1、选择题 下列实验中,不能观察到明显变化的是
A.把绿豆大的钾投入少量水中
B.把一段打磨过的镁带放入少量冷水中
C.把溴水加入到淀粉KI溶液中
D.氢气和氯气等体积混合后强光照射
参考答案:B
本题解析:略
本题难度:简单
2、实验题 某化学探究小组拟用铜片制取Cu(NO3)2,并探究其化学性质。
(一)他们先把铜粉放在空气中灼烧,再与稀HNO3反应制取硝酸铜。
(1)如果直接用铜屑与稀HNO3反应来制取硝酸铜,可能导致的两个不利因素是____________________________、___________________。
(2)实验中铜粉应该放在________(填“蒸发皿”、“坩埚”或“烧杯”)中灼烧。欲从反应后的溶液中得到硝酸铜晶体,实验操作步骤按顺序分别是________、_______、过滤。
(二)为了探究Cu(NO3)2的热稳定性,探究小组按下图中的装置进行实验。(图中铁架台、铁夹和加热设备均略去) 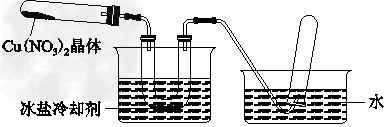
往左试管中放入研细的无水Cu(NO3)2晶体并加热,观察到左试管中有红棕色气体生成,最终残留黑色粉末;用U形管除去红棕色气体,在右试管中收集到无色气体。
(1)红棕色气体是________。
(2)当导管口不再有气泡冒出时,停止反应,这时在操作上应注意________________。
(3)探究小组判断Cu(NO3)2的分解属于氧化还原反应,产物除了红棕色气体和黑色固体外,进一步分析、推断,分解产物中一定还含有____________。
(三)为了探究Cu(NO3)2在酸性条件下跟铁单质的反应。他们取一支试管,加入Cu(NO3)2溶液,滴入适量稀硫酸酸化,再加入一定量铁粉,实验后没有固体残留物质。
(1)反应中最先起氧化作用的是__________。
(2)该探究小组对反应后溶液中铁元素的价态进行探究,他们设计了实验方案,并进行实验。请按下表格式补充写出实验操作步骤、预期现象与结论。 
参考答案:
(一)(1)生成等物质的量的硝酸铜,消耗硝酸原料多;产生污染物NO
(2)坩埚;蒸发浓缩;冷却结晶
(二)(1)NO2;(2)先把导气管移出水面,然后熄灭酒精灯火焰;(3)O2
(三)(1)HNO3(或H+和NO3-)
(2)不能;若KMnO4溶液的紫红色褪去或变浅,则说明产物中含+2价铁元素,若KMnO4溶液不褪色或不变浅,则说明产物中不含+2价铁元素;另取少量溶液,滴加KSCN溶液
本题解析:
本题难度:一般
3、选择题 下列实验设计方案中,可行的是
A.用碱石灰除去氯气中的水
B.在某试样中加入NaOH溶液,加热,产生能使石蕊试纸变红的气体即证明有NH4+
C.焰色反应实验中用硫酸清洗铁丝,灼烧后再沾取试样在酒精灯上灼烧观察
D.分液操作时 ,分液漏斗中下层液体从下口放出,上层液体从上口倒出
,分液漏斗中下层液体从下口放出,上层液体从上口倒出
参考答案:D
本题解析:略
本题难度:简单
4、填空题 在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示。
(1)该反应的化学方程式____________________________.
(2)该实验操作是将_______________滴加到___________另一种溶液中。
(3)当加入溶液的质量为ag时,所得溶液中的溶质为______________(写化学式)。
(4)当加入溶液的质量为bg时,向所得溶液中滴加酚酞溶液,溶液呈_____________色。
参考答案:(1)NaOH+HCl=NaCl+H2O
(2) NaOH 、HCl?(3)NaCl和HCl?(4)红
本题解析:本题以学生熟悉的中和反应实验为素材,进行了大胆的创新:一是用曲线图表示反应过程中溶液的pH变化情况,二是将中和反应实验与溶液知识相结合。考查的知识有化学方程式的书写、反应过程中溶液组成的判定以及酚酞在碱性溶液中呈现的颜色等。要求学生有较强的识图能力和思维能力,更有利于真正做过实验的学生作答。本题总体难度较大,但4个空有较好的梯度,兼顾了学生的基础性和发展性,具有较好的选拔功能。
(1)写盐酸和氢氧化钠溶液反应的方程式,比较容易;
(2)观察图,不难发现溶液的pH逐渐增大,而且最终大于7,说明操作是向盐酸中滴加强氧化钠。
(3)当加入溶液的质量为ag时,溶液显酸性,所以溶质为NaCl和HCl;
(4)只要学生掌握了pH与溶液酸碱度的关系以及酚酞溶液在碱性溶液中所呈现的颜色,作答并不难。当加入溶液的质量为bg时,溶液显碱性,所以滴加酚酞,溶液显红色。
本题难度:简单
5、选择题 下图中有关实验的操作方法或现象有误的是?(?)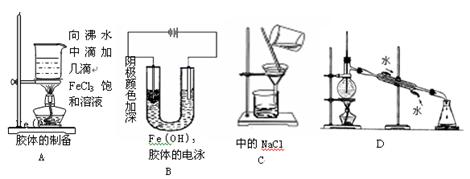
参考答案:C
本题解析:略
本题难度:一般